Historia de la Fisica Moderna Los Descubrimientos y Evolución
Historia de la Física Moderna - Siglos XIX y XX
Temas Relacionados:
1-Que es el Atomo y su Energía
2-Organismo Geneticamente Transformado
3-La Nanotecnología
4-Proyecto Genoma Humano
HISTORIA DE LA FÍSICA MODERNA - SIGLO XIX Y XX:
La física del siglo XIX creyó posible dar una solución sencilla a todos los problemas de la materia y de la energía.
Creía en principios que la parecían inviolables: invariabilidad de la masa, carácter inalterable e indestructible del átomo, transmisión de toda especie de energía en forma de ondas mensurables a partir de un determinado medio: el éter.
En 1865, James Clark Maxwell (1831-1879) publicó su célebre teoría electromagnética de la luz que demostraba magistralmente la identidad de las dos formas de energía luminosa y electromagnética.
La experiencia demostraría que, al igual que la onda luminosa, la onda electromagnética se refleja y se refracta.
Parecía como si se hubiese encontrado la solución definitiva de todos los problemas de la física generalizando el concepto de movimiento vibratorio y aplicándole los principios de la mecánica general.
Esta hermosa seguridad científica resultaría ilusoria.
Poco a poco fueron surgiendo inquietantes fenómenos que parecían dar al traste con las hermosas certezas sobre las que ya se comenzaba a descansar.
Primero fueron los rayos catódicos y la radiactividad,descubrimiento que circunstancias en parte fortuitas hicieron surgir a pocos meses de diferencia uno de otro y que eran la consecuencia de una larga serie de investigaciones cuyo origen se remontaba a unos doscientos años.
En la época de la electrostática, ya se habían interesado mucho por los fenómenos que acompañan el paso de la electricidad a través de los gases.
Después, cuando la antigua máquina de platillo fue reemplazada por la bobina de Ruhmkorff (1803-1877) y la ciencia del vacío se perfeccionó considerablemente gracias a los dispositivos que rehabilitaban la cámara barométrica y al gran empleo del mercurio, fue posible observar lo que pasaba cuando la descarga eléctrica se produjo en una atmósfera gaseosa rarificada.
Estaba reservada a sir William Crookes (1832-1919) realizar el más sensacional de los descubrimientos de su tiempo.
Hábil experimentador, Crookes se dedicó a estudiar, a partir de 1878, el paso de la corriente por tubos en los que el gas se reducía a algunas moléculas.
En estas condiciones, el interior de la ampolla no produce ninguna luz "mientras que sus paredes se iluminan con una viva claridad verde".
Tras una serie de ingeniosos experimentos, Crookes terminó por demostrar que se trataba de una irradiación particular emitida por el electrodo negativo o cátodo.
Esta irradiación se propaga en línea recta a través del tubo, hace luminiscentes y calienta los cuerpos sólidos que encuentra y hasta ejerce una presión sobre ellos.
Todo sucede, en fin, como si unos corpúsculos lanzados a gran velocidad bombardeasen los cuerpos más próximos.
A pesar de todas las ideas admitidas en su tiempo sobre la primacía de las ondas, Crookes tuvo la audacia de pensar que la luz verde que aparecía en las paredes de la ampolla no era otra cosa que un flujo de moléculas materiales lanzadas a gran velocidad.
No se equivocaba más que sobre la dimensión de los proyectiles pero volvía a introducir en física una noción pasada de moda y ridiculizada: la emisión.
¿Se habría equivocado Newton?
Entre tanto, todos los laboratorios de Europa se proveían de ampollas de Crookes.
Hacia 1880, demostró que los rayos catódicos—así se les llamaba entonces—atravesaban unas delgadas láminas de metal colocadas en su trayecto en el interior de la ampolla y en 1892 con guía Lénard hacerlos salir del tubo a la atmósfera sin otro artificio que el de practicar en la ampolla una ventanilla formada por una de esas delgadas láminas de metal.
Esto equivalía a arruinar la hipótesis de la emisión ya que ningún bombardeamiento molecular podía jactarse de atravesar las paredes, pero....¿y si los proyectiles no eran moléculas?.
La cuestión quedó zanjada por un experimento decisivo realizado en 1895 por Jean Perrin, entonces preparador en el laboratorio de la Escuela normal superior.
Perrin demostró que los rayos catódicos no son más que granos de electricidad negativa lanzados a gran velocidad a través de la ampolla vaciada.
En otros términos: acababa de descubrirse el electrón.
En este mismo año 1895, Roentgen (1845-1923) se entregaba, por su propia cuenta, a experimentos sobre los rayos catódicos cuando, por casualidad, observó que el tubo de Crooke: emitía otro género de irradiaciones.
Pues bien: se trataba de un hecho propiamente hablando escandaloso, ya que estos nuevos rayos se propagaban exactamente en línea recta, atravesando los cuerpos opacos y permitiendo fotografiar, a través de la carne, el esqueleto de un ser vivo.
Este descubrimiento estalló algo así como una bomba en todos los laboratorios del planeta.
No era difícil repetir el experimento: un tubo de Crookes, una bobina de inducción, una placa fotográfica envuelta en un papel negro. y una pantalla recubierta de una sustancia fluorescente.
Se hicieron muchas radiografías ; no faltaron los "cobayas".
Había dos cosas absolutamente desconocidas a propósito de estar misteriosas radiaciones, a las que inmediatamente se las bautizó como rayos X: primero el tremendo peligro que entrañan por poco que uno se exponga a ellos con demasiado frecuencia. y después su origen.
¿Por qué parte del aparato eran emitidos?
El gran matemático Henri Poincaré expresó la idea que quizá la emisión de rayos X estuviera ligada a la fluorescencia del vidrio herido por los rayos catódicos.
En esta teoría coincidían a la vez una verdad y un error; la pared de vidrio emite, en efecto, la misteriosa irradiación, pero esta emisión se opera sin conexión con la florescencia.
La emisión la realizan tan bien o mejor cuerpos que no son en absoluto fluorescentes.
Esta comprobación no parecía tener utilidad alguna, pero habría de llevar al descubrimiento de la radiactividad natural.
El 20 de enero de 1896, lunes, día de sesión en la Academia de Ciencias, Henri Poincaré mostró a sus colegas las primeras radiografías hechas en Francia y propuso la teoría antes aludida y según la cual el vidrio de la ampolla de Crookes, hecho fluorescente, había emitido rayos X.
Si las cosas se desarrollaban así. sustancias naturalmente fluorescentes como, por ejemplo, el sulfato doble de uranio o de potasio, debían producir espontáneamente rayos X.
Es lo que quiso averiguar Henri Becquerel (1852-1908).
Cogió un chasis opaco, de cartón negro, que contenía una placa fotográfica y dos láminas de sulfato doble de uranio y de potasio sujetas por unas tiras de papel.
Entre una de ellas y el chasis colocó una moneda de plata y lo expuso todo a los rayos del sol.
Al revelar la placa, Henri Becquerel comprobó que aparecían unas huellas correspondientes al emplazamiento de las láminas y de la moneda de plata que absorbían en parte las irradiaciones de las dos sustancias.

¿Quedaba confirmada la hipótesis de Henri Poincaré?.
¡Quién sabe!.
En espera de que llegara un día soleado que tardaba en presentarse, Becquerel encerró todo su equipo en un cajón oscuro.
Cuál no sería su sorpresa cuando el 1 de marzo de 1896 quiso asegurarse de que su placa fotográfica estaba todavía virgen.
Impulsado por no se sabe qué curiosidad, la desenvolvió y la encontró impresionada.
Ante sus ojos extrañados aparecieron con toda claridad unas sombras que dibujaban las formas de las láminas y mostraban la radiografía de una cruz de cobre muy fina colocada sobre una de ellas.
La sal de uranio emitía rayos X tanto en plena oscuridad como a la luz.
La fluorescencia no intervenía para nada en el fenómeno. Con una intuición admirable, Becquerel pudo anunciar entonces el hecho de que se trataba de una propiedad atómica independiente de la composición química del elemento uranio.
Acogida al principio con reticencia, esta tesis fue confirmada en febrero del año siguiente por J. J. Thomson y por su joven ayudante Ernest Rutherford, quienes estudiaron también los "rayos uránicos".

Gradualmente se iba imponiendo la verdad: las sales de uranio eran una especie de ampollas de Crookes naturales aun cuando nadie sabía decir por qué.
En 1882, Pierre Curie (1859-1906) fue nombrado jefe de trabajos prácticos de la Escuela de física y química.
En esta época, este gran científico y su esposa Marie (1867-1934) eran desconocidos del gran público, pero quienes estaban al corriente de los progresos de la física tenían ya a los dos esposos como unos genios.
Esposos Curie

Pierre Curie se ocupaba de cristalografía cuando la señora Curie tuvo la idea de investigar las propiedades del uranio en los diversos compuestos de este elemento y en los minerales que lo contienen.
Algunos de ellos demostraban una actividad mayor aún que la del uranio puro.
No era difícil sacar la conclusión de este fenómeno: estos minerales debían contener un cuerpo desconocido más activo que el uranio.
Pierre Curie se dio cuenta inmediatamente de que sus trabajos sobre cristalografía podían esperar un poco y que convenía trabajar sobre los datos recogidos por su esposa.
Poco después demostraba la señora Curie la existencia de un cuerpo nuevo: el polonio; después, los dos esposos redoblaron sus esfuerzos y pudieron anunciar, el 26 de diciembre de 1898, que habían descubierto un nuevo elemento que se desintegraba espontáneamente: el radio.
Más aún, Pierre y Marie Curie pudieron establecer muy pronto que el radio se transforma en otros productos radiactivos como el helio, para terminar finalmente en un metal inerte, el plomo.
Se había logrado una verdadera transmutación de elementos y este descubrimiento ha revolucionado el mundo.
En el terreno práctico, los resultados obtenidos por Fierre y Marie Curie iban a engendrar una muchedumbre de aplicaciones, sobre todo desde el punto de vista médico, pero hubo que esperar hasta 1912 para que se descubriera al fin en qué consistían los rayos X.
Utilizando las redes de moléculas descubiertas por Bravais, cristalógrafo francés del siglo XIX, y cuyas dimensiones del orden de la diezmilésima de miera son lo suficientemente pequeñas como para difractar los rayos X, el físico alemán Max von Laue reconoció al fin que estos rayos pertenecen al mismo grupo que los rayos luminosos ordinarios de los que no se diferencian más que por la extraordinaria rapidez de sus vibraciones.
Son, por así decirlo, hiperultravioleta, y en estas condiciones hubiera tomado nuevo vigor la tesis de las ondulaciones del éter si no hubiera descubierto Planck el fotón en 1898.
Max Planck

Ondas luminosas, rayos gamma y rayos X constituían, no cabía duda, emisiones de fotones.
La inexistencia del éter y, por tanto, de sus vibraciones, había sido ya realmente demostrada mucho antes, gracias a un experimento magistral.
En 1887 emprendió Michelson la tarea de demostrar el influjo de la translación terrestre sobre la velocidad de la luz.
Algunos años antes, en 1881, el ingenioso experimentador había inventado un interferómetro de una precisión inigualada.
Con ayuda de este aparato iba a poderse confirmar o destruir la existencia del éter.
En efecto, si este último es un medio estable que transmite los movimientos vibratorios, los de la onda luminosa o de la onda eléctrica, habría de poderse encomendar el movimiento de dos rayos de luz, uno de los cuales sería dirigido en el sentido de la traslación terrestre, el otro perpendicularmente al plano de este movimiento.
O dicho de otra forma, habría de poderse demostrar el desplazamiento absoluto de nuestro globo a través del éter por el complemento de velocidad de que se beneficiaría une de los rayos luminosos.
Ahora bien: la velocidad de la tierra es de unos 30 Km. por segundo, la de la luz de 300.000 Km. por segundo.
En estas condiciones, el desplazamiento de las franjas luminosas de interferencia debía corresponder a la ínfima diferencia de una cienmillonésima, fracción que representa el cuadrado de la relación entre la velocidad de desplazamiento de la tierra y la velocidad de la luz.
Michelson, con ayuda de su colega Morley, realizó un ingenioso dispositivo compuesto de cuatro espejos, una fuente luminosa y el interferómetro de precisión de que hemos hablado antes.
El resultado del experimento fue absolutamente negativo.
El suplemento de 30 Km. por segundo no aceleraba en modo alguno el rayo luminoso que continuaba imperturbablemente su carrera a una velocidad normal de 300.000 kilómetros por segundo.
No se necesitaba más para afirmar que no existía el éter.
Y de ahí nació toda la teoría de la relatividad.
ALBERT Einstein (1879-1955) hay que considerarle ante todo como matemático, pero como la física es una ciencia que se matematiza cada vez más, la relatividad constituiría para ella una fuente de fecundas explicaciones.
En primer lugar, como no puede encontrarse ningún punto fijo en todo el universo, había que admitir que el mundo en que vivimos está construido de tal forma que, en un sistema en movimiento, es imposible evidenciar el desplazamiento de ese sistema y a fortiori, la velocidad del mismo desplazamiento.

A este postulado, o más bien axioma, puesto que parece evidente por sí mismo, añadía Einstein que, cualquiera sea el sistema en traslación a partir del cual se mida la velocidad de la luz, esta velocidad conserva siempre el mismo valor numérico.
En el campo de la astronomía, la introducción de un constituyente limitado en un todo que se creía infinito iba a imponer inmediatamente la noción de un universo cuyas fronteras, siempre móviles, han sido establecidas recientemente sobre la base de un radio de diez mil millones de años-luz.
En física, había que concluir que la inexistencia del éter terminaba con las viejas leyes de la cinemática clásica y que la noción de espacio, tomada aisladamente, ya no tenía ningún sentido.
Esto llevó a Einstein a la noción muy abstracta de continuum espacio-tiempo y a la aceptación por parte de los físicos de una hipótesis propuesta ya en el siglo pasado por Riemann y que negaba que el espacio fuese independiente de los fenómenos físicos que se desarrollan en él, lo que necesariamente hacía del tiempo una dimensión del espacio.
La física nuclear ha demostrado en nuestros días que esta noción respondía a la realidad.
Sabemos experimentalmente que la energía posee una masa y que la masa se materializa en energía, principio expuesto por Einstein ya en 1905 y que se resume en esta fórmula clave de nuestro mundo moderno: E = mc2, en la que la energía equivale a la masa multiplicada por un factor correspondiente al cuadrado de la velocidad de la luz.
Los descubrimientos de Einstein no se agotan ahí.
Aprovechando las conclusiones impuestas por unos experimentos realizados en 1903 con el tubo de Crookes, Einstein afirmará que la verdadera masa del electrón no es de naturaleza mecánica, sino de naturaleza electromagnética.
En estas condiciones, los fenómenos electromagnéticos se imponían a todos los demás y sus leyes vendrían a constituir los principios básicos de la mecánica.
Con la formulación de la relatividad restringida se abre el camino a la tesis que Einstein desarrollará más tarde en forma de una teoría de la relatividad generalizada.
Todo esto teniendo en cuenta el concepto del danés Bohr, quien en 1913 rechazará el electromagnetismo clásico en su concepción del modelo de átomo, lo que apunta claramente hacia el camino que más tarde conducirá a los físicos a considerar favorablemente la gran hipótesis del campo unitario.
Al mismo tiempo, una nueva teoría tan desconcertante como la de la relatividad iba a dar al traste con la hermosa noción de continuidad, sobre la que descansaba la física clásica.
Se trata, naturalmente, de la teoría de los quanta, formulada muy ingeniosamente hacia 1900 por el gran físico alemán Max Planck por razones puramente experimentales: la famosa emisión de luz por los cuerpos negros, verdadero rompecabezas para los físicos de la época.
Las teorías de Planck revisten un grado tal de abstracción que nos es imposible explicarlas aquí, porque se necesitaría todo un capítulo especial cargado de fórmulas y gráficos.
Lo esencial es saber que, según Planck, toda especie de energía es de naturaleza discontinua.
O dicho de otro modo: la luz o la electricidad no nos las proporciona la naturaleza en forma de flujo ni de fluido, sino, literalmente hablando, en pequeños paquetes: los quanta.
Para no dejar nada al azar, Planck se tomó el cuidado de cifrar con la mayor exactitud las dimensiones de esos paquetitos.
En unidad C. G. S., se expresa con el número cuasi infinitesimal de 6,55 X 10-27.
No podría irse más lejos, y ésa es, en efecto, la medida exacta de un simple grano de energía simbolizada por la letra h, o constante de Planck.
Los intercambios de energía entre materia e irradiación se hacen, pues, por quanta.
La irradiación tiene una estructura discontinua, lo mismo que la emisión, sobre todo la emisión de la luz.
Se recordará que apoyándose en la teoría de los quanta descubrió Einstein en 1905 el fotón o grano de luz.
Esto produjo un gran escándalo ya que venía a derribar los cálculos de los hombres de ciencia.
Si la luz era una emisión de fotones y la electricidad una emisión de electrones, ¿cómo explicar la continuidad que es la ley de las ondas?.
La dificultad la resolvió en 1924 otro gran genio científico, Louis de Broglie, nacido en 1892 y Premio Nobel de física en 1929.
Como ha dicho él mismo, lo esencial era encontrar un sujeto al verbo ondular.
Louis de Broglie pensó que ese sujeto tenía que ser el mismo electrón y no ese éter demasiado metafísico.
"Si así fuera, dice el gran científico, habría que pensar que hay que imaginarse los corpúsculos materiales, especialmente el electrón, como acompañados, y en cierto sentido guiados, por una especie de onda". Esta solución de compromiso es la base de la nueva doctrina llamada ondulatoria.
Desde ese momento ya no existe el escándalo. "Hoy sabemos que el protón y los núcleos de los átomos, en los que están concentradas las cargas positivas de la materia, están también asociados a ondas... por lo que la barrera que, desde hacía tanto tiempo, separaba la física de las radiaciones de la física de la materia parece haberse derrumbado ya."
Así lo que quiere esta nueva doctrina de una abstracción impresionante.
Desde ese momento, la realidad física va a volatilizarse en un "esquema matemático", para servirnos de la expresión de Sommerfeld, y la ciencia, a medida que se va desarrollando, se alejará cada vez más del "antropomorfismo de la sensación".
En 1897, el gran físico inglés Joseph J. Thomson (1856-1940) cuando estaba perfeccionado el experimento de Lénard (1885) sobre los rayos catódicos, descubrió que estos extraños rayos podían ser deflectados por medio de un electroimán.
Calculó su velocidad y encontró que era muy próxima a los 300.000 Km. por segundo; después, suponiendo que estaban compuestos de corpúsculos, trató de estimar la masa y la carga de éstos.
Pudo establecer que la relación de la carga a la masa de la partícula era una constante independiente a la vez de la naturaleza del gas contenido en la ampolla y del metal de los electrodos.
"No veo, dice, forma alguna de escapar a la conclusión de que se trata de cargas de electricidad negativa transportadas por partículas de materia."
Desde entonces pasó a ser de dominio público el término electrón.
En 1909, Robert Millikan, profesor entonces de la Universidad de Chicago, acometió la tarea de demostrar experimentalmente la existencia y la naturaleza de la partícula.
El dispositivo que inventó era de una genial sencillez: consistía en una cámara de niebla en la que unas gotitas de aceite en suspensión subían o bajaban según que obedeciesen a la simple gravedad o al impulso de un campo magnético variable.
Un excelente aparato óptico permitía observarlas cómodamente. De cuando en cuando, una gotita cambiaba brutalmente de velocidad.
¿No sería porque había capturado un electrón?
En este supuesto, como se conocía la masa de la gotita y la intensidad del voltaje, resultaba teóricamente posible deducir la carga del electrón y también su masa.
Pero el electrón es tan pequeño que la gotita cargada con veintidós partículas se comportaba exactamente como si sólo estuviese cargada de una.
Expresada en culombios, la carga de un electrón implica dieciocho ceros antes de la coma.
En cuanto a la masa, necesita veintisiete ceros antes del primer decimal.
Puede suponerse los esfuerzos que tuvo que hacer el ingeniero físico para llegar a esos resultados, pero de todas maneras, el electrón no era un mito, aun cuando, según la expresión del mismo Millikan, el radio de un cabello comparado con el de mi electrón sea aproximadamente diez mil millones de veces más grande.
El descubrimiento del protón no se realizó oficialmente hasta 1920, pero hacía ya mucho tiempo que rondaba la mente de los científicos.
En 1886, el físico alemán Goldstein colocó en el centro de un tubo de Crookes un ánodo constituido por un enrejado muy fino y no sólo pudo observar la aparición de rayos catódicos, sino también la de una radiación de un amarillo dorado claro que "penetrando el enrejado, llenaba todo el espacio entre el cátodo y la pared.".
Esta radiación no era otra cosa que una emisión de protones, partículas nucleares cuyo peso es igual al de 1.840 electrones.
La irradiación de Goldstein contenía núcleos de nitrógeno puro.
Si el gas rarificado de su tubo hubiera sido de hidrógeno, su color hubiese sido rosa, verdoso o grisáceo si hubiese sido de óxido de carbono.
En realidad, Goldstein no había hecho más que ionizar el gas de su ampolla, es decir descomponer los átomos de este gas en electrones (rayos catódicos) y en protones (rayos canales).
En 1910 volvió J. J. Thomson a hacer la experiencia y terminó por proyectar los misteriosos rayos canales sobre una pantalla fluorescente en la que producían unas escintilaciones del mismo tipo que las de los electrones.
Con ayuda de un electroimán, el experimentador podía deflectar la irradiación y reunir en una misma parábola las partículas del mismo peso atómico.
Entonces se produjo la gran sorpresa.
Thomson había utilizado el neón y descubrió que de su cátodo abierto se desprendía una doble radiación positiva.
"No cabe duda de que lo que llamamos neón no es un gas simple, sino la mezcla de dos gases, uno de los cuales tiene un peso atómico 20 y el otro un peso atómico 22."
Sin darse cuenta, Thomson acababa de descubrir los isótopos que en 1920 separó entre sí su colaborador Aston con ayuda de su espectrógrafo de masa.
Entre tanto, el estudio de la radiactividad natural iba a llevar a los científicos a realizar una hazaña con la que habían soñado los alquimistas de la Edad Media.
En 1903 habían demostrado sir Frederik Soddy y sir William Ramsay que la radiactividad del radio iba acompañada de un desprendimento de helio.
En 1907, Rutherford pudo establecer definitivamente la identidad de la partícula alpha con el átomo de helio ionizado, es decir, privado de sus dos electrones satélites, o dicho de otra manera del helio.
En 1919, Rutherford concibió la excelente idea de bombardear átomos de nitrógeno con ayuda de helios que circulaban a gran velocidad y emitidos en forma de rayos alpha por una sustancia muy radiactiva.
Observó que de esta forma el nitrógeno se transformaba en oxígeno.
Por primera vez, se había roto un átomo y sus elementos constitutivos habían engendrado otro cuerpo simple.
¡La transmutación no era ya un sueño de alquimista!
Rutherford había salido airoso donde Bacon y Paracelso habían fracasado.
En 1913 emprendió Niels Bohr (1885-1962) la tarea de cuantificar el átomo.
Adoptando el modelo de Ernest Rutherford y Jean Perrin, en otros términos, conservando las órbitas keplerianas circulares como trayecto ideal de los electrones, se dedicó a establecer un valor matemáticamente riguroso de todos los estados posibles de estas partículas ínfimas.
Demostró sobre todo que pasando de un estado estacionario n1 a otro estado estacionario n2, el electrón emite un quantum de energía. Acababa de desvelarse el misterio de la electricidad.
La experiencia no tardó en confirmar la exactitud de esta aplicación genial de las teorías de Planck.
Pero como las órbitas circulares de los electrones presentaban serios inconvenientes, Sommerfeld reanudó en 1916 el trabajo de Bohr dando una forma elíptica a estas órbitas y utilizando los principios de la relatividad para tratar del movimiento de los electrones sobre sí mismos.
Dejemos ya el terreno de la pura teoría para volver a la desintegración del átomo.
El principio según el cual se da cierta disipación de masa en algunos bombardeos atómicos, y esto en las condiciones previstas por Niels Bohr y Sommerfeld, iba a conducir a los científicos hacia una pista al mismo tiempo gloriosa y peligrosa.
Hacia 1930 se advirtió que cuando se efectuaba una transmutación se liberaba una gran cantidad de energía. En efecto, los núcleos de los elementos formados tienen una masa menor que la de los elementos constitutivos.
Por tanto, hay algo que se disipa durante el proceso.
Y si la pérdida de masa equivale al aniquilamiento de un solo gramo de materia, la energía liberada es igual a una cantidad de calor suficiente para hacer hervir instantáneamente 200 millones de litros de agua.
En cierto sentido , no había en ello nada de nuevo, ya que no era más que la aplicación de la célebre fórmula de Einstein E = mc².
Todavía faltaba por encontrar el proyectil que pudiera producir desintegraciones eficaces.
Los alemanes Bothe y Becker y los franceses Frederic Joliot e Irene Joliot-Curie estudiaron la desviación sufrida por los rayos alpha cuando atraviesan delgadas capas de materia, y se observó que las partículas alpha que bombardean un metal ligero pero resistente, el berilio, originaban una irradiación paradójica, capaz de romper las más fuerte barreras de potencial y "de moverse libremente a través de la materia", como había predicho Rutherford en 1920.
Entonces fue cuando James Chadwick pudo precisar en 1932 que esta irradiación debía estar constituida por partículas neutras de masa próxima a la del protón.
Estaba descubierto el neutrón, la bomba atómica y la energía nuclear vendrían más tarde.
Entre tanto se había inaugurado la era de los desintegradores de átomos.
Pretender alcanzar los núcleos atómicos con corpúsculos alpha, como lo habían hecho el matrimonio Curie y James Chadwick, equivalía a "disparar con carabina sobre cabezas de alfiler sembradas de 10 en 10 metros".
Por supuesto que podían reemplazarse estos corpúsculos alpha por protones, pero, ¿cómo imprimir a éstos una velocidad suficiente?.
Desde 1931 había en la Universidad de Princeton un generador electrostático inventado por Robert van de Graaff y cuyo principio no difiere sensiblemente del de la máquina deWimshurst.
La aceleración de los protones se produce con ayuda de un transformador de alta tensión, situado en la base del aparato y que alimenta un peine que deposita sobre una correa que desfila bajo sus dientes cargas eléctricas que, transportadas hacia la parte superior del aparato, son recogidas por un peine colector.
De esta forma se crea entre la base y la parte superior del dispositivo una diferencia de potencial de 80.000 V. en el primer modelo y llegó a 6 millones de voltios en las bombas del gigante instalado en Round Hill algunos años más tarde.
Ya en 1930, Ernest Orlando Lawrence había realizado otro aparato que habría de destronar poco a poco a los grandes aceleradores lineales: el ciclotrón.
El principio es bastante simple: en el centro de un recipiente cilíndrico en el que unas bombas producen un vacío lo más perfecto posible se inyectan partículas atómicas bajo débil energía.
Se coloca entre los polos de un electroimán, lo que engendra en su interior un campo magnético intenso.
Las partículas comienzan a girar en círculo, aceleradas a cada vuelta por los electrodos elevados a potenciales de muy alta frecuencia.
Atraídas de un electrodo a otro, las partículas describen así una espiral a una velocidad creciente.
Finalmente son desviadas hacia un blanco que contiene la sustancia que ha de ser bombardeada y desintegrada: berilio por ejemplo.
Nuestros ciclotrones actuales permiten acelerar partículas a velocidades próximas a la de la luz y disponen así de energías suficientes para romper cualquier núcleo de átomo.
En 1932 no podía pensarse aún en estos esplendores. John D. Cockcroft y E. T. S. Walton, en el laboratorio Cavendish, tuvieron que contentarse con un duplicador de voltaje de 150.000 V. A fuerza de ingeniosidad consiguieron obtener 700.000 V. y terminaron por desintegrar núcleos de litio en dos helios, utilizando como proyectiles protones acelerados.
Gracias a la cámara de niebla inventada por C. R. F. Wilson entre 1899 y 1912, las partículas resultantes de la desintegración del litio pudieron ser localizadas por los experimentadores.
Todos los manuales de física han reproducido el cliché de la desintegración del litio por Cockcroft y Walton.
Todavía hoy nos impresiona este auténtico documento histórico.
El neutrón fue identificado en 1932 por Chadwick, lo que algunos años después permitiría la fisión nuclear.
Había nacido un nuevo modelo de átomo.
Todo núcleo aparecía como constituido de nucleones, es decir, de partículas positivas: los protones, y de partículas neutras: los neutrones.
En torno a este agregado increíblemente denso de nucleones gravitan los electrones satélites cuyas cargas negativas, al menos en un átomo en equilibrio, equivalen rigurosamente a la suma de las cargas positivas de los protones.
Sucesivamente, el núcleo del átomo se iría enriqueciendo con partículas ligeras: mesones, neutrinos, etc., sin hablar de las partículas de antimateria de que se hablará más adelante.
Volviendo a la fisión nuclear, el proyectil ideal resultaría ser el neutrón y el blanco elegido el uranio.
El 14 de abril de 1934, Enrico Fermi descubrió que los neutrones ralentizados en la parafina provocan otras desintegraciones en el interior de otros átomos.
Para llegar a la desintegración en cadena había que frenar la velocidad de los neutrones, transformarlos en neutrones térmicos.
Esa es la misión del grafito y del agua pesada; pero no adelantemos los acontecimientos.
Fermi Enrico

El 15 de enero de 1934, los esposos Joliot-Curie provocaron la estupefacción de la Academia de Ciencias anunciando que acababan de descubrir la radiactividad artificial.
Gradualmente se iban dando los pasos hacia la comprobación de que es posible introducir neutrones suplementarios en el interior de los núcleos y hacer fuertemente radiactivo un inocente fragmento de fósforo, de carbono o de cobalto.
Habían nacido los radioisótopos y todo el mundo sabe lo mucho que se los utiliza en medicina y en industria.
No era eso sólo. En 1939 estalló una verdadera bomba en el mundo de la ciencia: Otto Hahn, Lisa Meitner, Strassmann y Frisch habían descubierto que el núcleo del uranio convenientemente bombardeado con neutrones se-rompe en dos liberando una energía de 100 millones de voltios.
En su comunicación a la revista británica Nature del día 16 de enero, Lisa Meitner explicaba que, al igual que la gota de agua que ha ido creciendo, el núcleo de uranio no podía ya resistir y... explotaba.
Lo que ha sucedido después es ya del dominio público. No hablaremos de la batalla del agua pesada ni de la angustiosa rivalidad que enfrentó durante cinco años a los Aliados y al III Reich.
Recordemos simplemente que a comienzos de 1940, el ingeniero Nier separaba, en la Universidad de Minnesota, del uranio-238 su precioso isótopo, el uranio-235; por supuesto que a una escala infinitesimal.
Y que en 1941, el ilustre Fermi, premio Nobel de 1938, se instalaba en Chicago en donde montaba su primera pila atómica, que comenzó a "diverger" el 2 de diciembre de 1942, produciendo por primera vez dos elementos transuranianos: el neptunio y el plutonio, que ya en 1940 habían descubierto McMillan y Seaborg.
Recordemos también el famoso Manhattan Project, la primera explosión atómica del 16 de julio de 1945 en Alamogordo, y finalmente, las hecatombes nucleares de Hiroshima y Nagasaki, los días 6 y 9 do agosto de 1945.
Como instrumento de muerte repentina, la bomba A era ya aceptablemente eficaz, pero más lo seria la bomba H "encendiendo sobre la tierra el fuego del sol y de las estrellas".
He aquí algunas explicaciones.
Ya en 1934, algunos científicos habían reconocido el principio de la fusión del hidrógeno en helio, como fuente posible de energía.
Una simple sustracción bastaba para demostrar que la reacción: 2/H + 2/H = 4/2 He era "viable".
En efecto, dos núcleos de hidrógeno pesado dan en conjunto 4,02516 unidades de masa mientras que el núcleo de helio que resultará de su "fusión" no tiene más que 4,00390.
Hay, pues, un excedente de materia; 0,02126 unidad de masa y este excedente se traduce en una liberación de energía correspondiente a 500.000 KW/h. por cada molécula-gramo de helio.
Como esta reacción parecía más bien del dominio de un porvenir muy lejano, nadie habla de ella antes de 1950, excepción hecha del físico Vienes Hans Thirring, quien en 1946 la consagró un estudio bastante notable.
Ver: Energía de la Fisión Nuclear
En noviembre de 1952, el mundo quedó aterrado al saber que una bomba termonuclear de al menos 7 megatones había estallado en Eniwetok, haciendo desaparecer una isla de la superficie del mar y cavando en su lugar un embudo de 2 Km. de diámetro y 60 m. de profundidad.
Después vino la demostración del 1º de marzo de 1954, en la que cinco pescadores japoneses fueron contaminados por la caída del polvo radiactivo (lluvia radiactiva).
¿Esta "Kraftprobe" tuvo el mérito de poner a científicos e ingenieros sobre la pista de un tipo de reactor más rentable que los de uranio que surgen por todas partes propulsando incluso submarinos y rompehielos atómicos?.
Sólo el futuro nos lo dirá.
La mayor dificultad que hay que vencer es la obtención de una temperatura llamada de fusión del orden de varios centenares de millones de grados; una proeza que es realizable durante una fracción de segundo, por medio de una prebomba de uranio, pero de la que todavía no son capaces ni la ingeniosa Zeta británica ni el extraordinario Slellarator americano.
Sin embargo, los métodos de "striction" y de "confinamiento" de un plasma que consiguen ya de 2 a 3 millones de grados no han dicho su última palabra, aun cuando los progresos hayan sido muy lentos desde 1958.
Volviendo ahora a la física pura, la encontraremos esencialmente ocupada en explorar este mundo extraño que es el núcleo del átomo y esa verdadera fantasmagoría que es la materialización de la energía.
¿Cómo explicar la paradójica densidad del "nucleus" y de las fuerzas que dan cohesión a los nucleones?.
Nada permite pensar que sean de naturaleza eléctrica.
Cuando en 1935 emitió el físico japonés Yukawa la hipótesis de un intercambio de mesones entre los protones y los neutrones de un núcleo, se vio obligado a admitir que estas partículas debían tener una masa 200 veces mayor que el electrón, pero que su "vida" era muy breve, de apenas una millonésima de segundo.
En mayo de 1937, el estudio de los rayos cósmicos en la cámara de Wilson revelaba la existencia de dos mesones, el segundo de los cuales asegura la cohesión de los nucleones entre sí, mientras que el primero parece escaparse por la banda dando nacimiento a un electrón.
Diez años más tarde, durante el invierno 1947-1948, el gran sincrociclotrón de la Universidad de Berkeley consiguió producir mesones ir cuya trayectoria terminaba, sobre la placa fotográfica, en una soberbia estrella, prueba de que el mesón había encontrado un núcleo y que lo había hecho estallar.
¿Qué había sucedido?.
Entonces surgió la pregunta de si no se habría producido algo más y de si la violencia de la explosión no supondría la presencia de una de esas antipartículas que, por simples deducciones matemáticas, había previsto el físico inglés Pirac en una nota dirigida a la Sociedad Real de Londres con fecha 6 de diciembre de 1929.
La ecuación era tentadora. Podría representársela así:
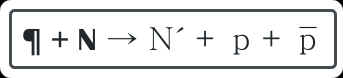
en la que ¶ es un mesón pesado o, como se dice técnicamente, un hiperón, N un nucleón cualquiera, p un protón normal, es decir positivo, y p´ un protón negativo o antiprotón.
Por supuesto que el par p y p´ no podían subsistir juntos sino que se aniquilaban recíprocamente.
En 1935 hubo quien pensó que el intermedio del mesón ¶ no hacía más que complicar las cosas y que, si se dispusiera de unos seis mil millones de electrones-voltios, quizá se pudiera crear directamente un "par" conforme a la fórmula siguiente:
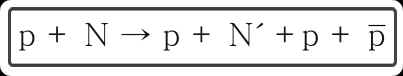
Esta fórmula fue realizada en el laboratorio de Berkeley el 24 de octubre de 1955.
En el estudio de la radiación cósmica, fue una primera figura mundial el meteorólogo español A. Duperier, quien descubrió el "efecto positivo" de la radiación y contribuyó con una de las más importantes aportaciones al campo de la física en los últimos años con el cálculo de los fenómenos de interacción entre las partículas dotadas de altísima energía, y sus trayectorias, que expuso en el Congreso Internacional de Edimburgo de 1958.
El descubrimiento del antineutrón, aunque erizado de dificultades, pudo realizarse en una fecha difícil de determinar.
En cuanto al electrón positivo o antielectrón, había sido descubierto antes de la segunda guerra mundial, ya que la obtención de un par (e y é) no exigió más que una energía relativamente baja, del orden de 1.0 millón de electrón-voltios aproximadamente.
El neutrino y el antineutrino han venido a completar la serie de los leptones o partículas ligeras.
Atisbado unos veinticinco años antes por el físico Pauli, el neutrino no fue descubierto hasta 1958 gracias a los escintiladores instalados en Savannah River.
¿El neutrino es la partícula que, en el campo gravitatorio, corresponde al electrón en el campo electromagnético?.
Quien viva lo verá.
Entre tanto, los físicos trabajan a contra reloj para descifrar los secretos de la materia y de la antimateria.
Enormes aparatos han entrado en funcionamiento, especialmente el gran sincrotrón de protones del CERN (Centro Europeo de Investigaciones Nucleares).
En 1961, este instituto procedió a millares de experimentos y tomó millón y medio de clichés que están actualmente en proceso de análisis.
Parece que se trata sobre todo de estudiar las interacciones de altas energías que implican las diversas especies de mesones, ya que ahí es donde en definitiva reside el secreto del átomo y del antiátomo.
¿Hacia dónde se encamina la física?.
El eminente científico francés Leprince-Ringuet confiesa que no sabe nada al respecto.
"Os diré únicamente, declaraba, que estamos trabajando pero sin saber exactamente lo que vamos a hacer y, en el fondo, eso es lo agradable."
Concepto Descriptivo Sobre la Conservación de la Energía






