Carga Electrica del Electrón Experimento de Millikan Vida y Obra
Carga Eléctrica del Electrón
Experimento de Millikan
El nombre de Roberto Andrés Millikan estará ligado para siempre al estudio de los electrones, las diminutas partículas cargadas de electricidad negativa que barren en torno el núcleo de cada átomo.
A partir de 1910, llevó a cabo una serie de ingeniosos experimentos en los cuales se dedicó a medir la carga que posee el electrón y confirmar que se trata de "la menor carga que puede existir".
Anteriormente, J. J. Thomson había determinado la relación de la carga de un electrón con su masa (e/m) y dedujo por electrólisis la carga sobre el ion de hidrógeno (un átomo de hidrógeno que ha perdido su único electrón), Millikan logró probar que, como era de esperar, la carga negativa sobre un electrón es de igual valor a la positiva que posee el ion de hidrógeno.
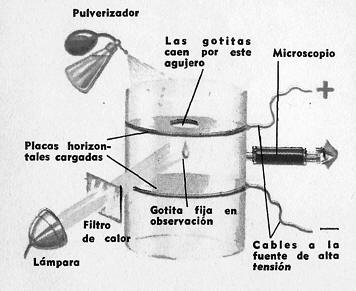
El experimento de Millikan consistía en inyectar gotitas de aceite con un pulverizador de perfume dentro del espacio comprendido entre dos placas metálicas paralelas y horizontales.
Dichas placas se hallaban conectadas a los terminales de una fuente eléctrica de alta tensión, de tal manera que una de ellas estuviese cargada positivamente y la otra negativamente.
Las gotitas eran iluminadas brillantemente (a través de un filtro que eliminaba el paso de rayos térmicos que de otra manera podrían establecer corrientes por convección) y las observó con un microscopio horizontal.
Al pasar por el chorro del pulverizador, la mayor parte de las gotitas se cargaban eléctricamente por la fricción.
En otras palabras, cada gotita había ganado o perdido algunos electrones.
Las que no lo habían logrado, podían ser cargadas con la ayuda de un haz de rayos X proyectado sobre ellas.
Las gotitas, por estar cargadas, eran atraídas hacia arriba o hacia abajo por la plancha de carga contraria. Supongamos que era atraída hacia arriba.
La fuerza de atracción se ajustó cuidadosamente regulando la tensión de la corriente aplicada, hasta que equilibraba exactamente el peso de la gotita.
En este caso, observada ésta al microscopio, pendía en el aire.
La fuerza de atracción depende de la distancia que hay entre las placas, la tensión de la fuente eléctrica (ambas pueden medirse con facilidad) y la carga que posee la gotita.
En consecuencia, para una gotita estacionaria podrá calcularse la carga siempre que se conozca la masa.
Hallar la masa de una sola gotita era lo más difícil del experimento.
La masa de todo objeto es igual al producto del volumen por la densidad.
Millikan logró hallar la densidad de un aceite determinado que usó en varias formas y pudo comprobar que las gotitas eran perfectamente esféricas.
El volumen de la esfera está dado por la fórmula 4.Pi.R3/3 donde r es el radio.
En consecuencia, era necesario medir el radio de una gota para determinar su masa.
Se equipó el ocular del microscopio con una escala, pero este recurso no resultaba realmente exacto para medir el ínfimo radio de una gotita.
Así, pues, Millikan tuvo que encontrar el radio apelando a un método indirecto. Desenchufó la corriente, de modo que la gotita se hundió por gravedad.
Con la ayuda de un cronógrafo midió la velocidad constante a que avanzaba ante su campo visual.
Avanzaba a una velocidad fija debido a que su peso era equilibrado por la resistencia del aire por el cual caía.
Existe una fórmula muy sencilla que relaciona la fuerza retardante (resistencia del aire) que actúa sobre una esfera que avanza constantemente, con su radio, la que suministró a Millikan el radio de la gotita que estaba investigando.
Al fin este investigador logró toda la información que necesitaba para medir la carga existente sobre una gotita de aceite.
Entonces repitió el experimento centenares de veces y obtuvo gran cantidad de resultados diferentes.
Esto no quiere decir que el experimento tuviese errores.
Era simplemente que las diferentes gotitas ganaban o perdían distintas cantidades de electrones.
Todos los resultados demostraron ser simples múltiplos (entre 5 y 20 veces) de una carga básica.
Esta carga básica resultó ser el máximo común múltiplo de cientos de resultados.
No se encontró carga menor en los experimentos de Millikan ni en ninguno de los subsiguientes.
Ésta es, en efecto, la carga soportada por un solo electrón.
Cada electrón lleva precisamente esta cantidad de carga, ni más ni menos.
Millikan ha medido con considerable exactitud una de las constantes fundamentales del Universo.
Roberto Millikan era estadounidense, nacido en Illinois en 1868. Después de cursar estudios en el Colegio de Oberlin, en la Universidad de Columbia en Berlín y Gotinga, llegó a profesor de física de la Universidad de Chicago.
En reconocimiento de sus trabajos sobre el electrón, recibió el Premio Nobel de Física en 1923. Inspirado maestro y autor en amplios temas científicos, Roberto Millikan falleció en 1953.
ESTRUCTURA ELECTRÓNICA DEL ÁTOMO
Hasta el año 1914, mucho habían discutido los físicos y los químicos acerca de la imagen del átomo, que, evidentemente, ya no podía concebirse como la más pequeña partícula de la materia que puede existir, sino como un verdadero edificio más o menos complicado.
Hoy se acepta universalmente la estructura enunciada por el francés J. Perrin (1901) expuesta claramente por el inglés Rutherford, y demostrada matemáticamente para algunos átomos, dando una acertada explicación de los espectros de emisión, por el danés Neis Bohr.

Esta estructura, que se asemeja a un sistema planetario, considera dos zonas en el átomo: la cortical (externa) y el núcleo.
La zona cortical o externa del átomo está formada por "electrones", corpúsculos cuyo peso es igual a 1/1.850 del peso del hidrógeno y giran alrededor de la parte central o núcleo.
El peso casi total del átomo está concentrado en el centro o núcleo del átomo, formado por protones y neutrones.
Fuente Consultada:
Revista TECNIRAMA N°56
El Estallido Científico en el Siglo XX Trevor Williams
Enlace Externo: Millikan, El Cientíifico Que Vió Al Electrón






