Historia del Origen de los Elementos Quimicos en la Tierra
Origen de los Elementos Químicos en la Tierra
¿Como se Formaron?
Explica Isaac Asimov en su libro Breve Historia de la Química, que el hombre primitivo utilizaba instrumentos naturales tal como los encontraba. Una rama podía ser un excelente garrote y una piedra, un inmejorable proyectil. Con el tiempo, descubrió nuevos materiales y aprendió a tallarlos y a pulirlos. Sin embargo, las piedras y maderas no modificaban su composición.
Hacia el año 8000 a.C. se produjeron otros cambios: el hombre aprendió a criar animales y a cultivar las plantas, dejó de ser nómade y se hizo sedentario, considerándose este hecho el comienzo de la civilización.
Mas tarde el hombre descubrió los primeros metales... las ventajas de estos materiales fueron aprovechadas con rapidez: el cobre, que fue el primer metal explotado, resultaba un material maleable y resistente. El hombre advirtió que podía obtenerlo a partir de unas piedras azuladas. Mayor aún fue su asombro cuando, al calentarlo con otro metal, el estaño, obtuvo una mezcla sorprendente: el bronce, que le dio nombre a la etapa siguiente: Edad del Bronce.
Pero la historia no quedó allí: fue descubierto un nuevo metal, el hierro, que aunque escaso resultaba más duro que el cobre. Se inicia así la Edad del Hierro: en esta etapa el desafío fue el perfeccionamiento de las técnicas de fundición, a través de las cuales se pudo extraer hierro de las "piedras" que lo contenían.
Pero bien, la inquietud que nos nace a partir de lo antedicho,...todo ese material usado por el hombre desde su descubrimiento hasta nuestros días, donde incluisve todavía hoy se les encuentran nuevas propiedades y nuevos usos tanto industriales como hogareños, ¿como han llegado a la corteza de nuestro planeta?...¿como se formaron?,...¿en que momento de la historia geológica?,...¿bajo que condiciones aparecieron?.
Una respuesta puede aparecer con solo mirar hacia arriba, hacia el cielo profundo, y pensar que el Universo está constituido por miles de millones de galaxias, sistemas que a su vez contienen miles de millones de estrellas, polvo cósmico y nubes de gases.
Pero, ¿como se formo el Universo? ...¿Cuáles son los elementos químicos que lo componen?.... ¿Podemos contestar estas preguntas?
Esta inmensidad hace que no resulte fácil conocer la cantidad y naturaleza de la materia que lo conforma. Todo permite suponer que la materia que forma los cuerpos celestes, y de la cual se tienen datos, constituye sólo un 10% del total de materia existente.
El 90% restante se denomina materia oscura; su estudio se hace muy difícil, pues tiene la característica de que no emite ni absorbe luz y escapa a los métodos de detección.Una de las pocas manifestaciones de esta materia invisible es la interacción gravitatoria que tiene con las estrellas y galaxias.
Estudiando la composición química del 10% de la materia conocida se concluye que el elemento más abundante del Universo es el hidrógeno (H); los restantes se formaron a partir de sucesivas fusiones de núcleos de aquél.
Los de mayor interés para la evolución química y el origen de la vida son: el carbono (C), el nitrógeno (N), el oxígeno (O), el fósforo (P), el azufre (S) y algunos metales como el hierro (Fe), el magnesio (Mg), el sodio (Na), el potasio (K) y el calcio (Ca), que junto con el hidrógeno constituyen los elementos biogénicos.
Llamamos elemento, y mas precisamente elemento quimico a la materia formada por un solo tipo de atomos, por ejemplo si tomamos una muestra de potasio (K) y dividimos por la mitad sucesivamente, cada porción analizada tendra siempre atomos de potasio, hasta que la misma tenga el tamaño mínimo atómico.
La materia se creó durante una violenta explosión (Big Bang) hace unos quince mil millones de años. En una pequeñísima fracción de segundo, los quarks, recién constituidos, se aglomeraron en protones, y éstos, a su vez, se fusionaron para formar núcleos de átomos de helio y de hidrógeno.
Las fuerzas gravitatorias acentuaron las irregularidades existentes en esta primigenia sopa y aglutinaron las regiones más densas hasta dibujar un inmenso tapiz cósmico de galaxias y vacíos (polvo interestelar).
A partir de las densas nubes de gas presentes en el seno de las galaxias nacieron las estrellas.
Pero, ¿cómo surgieron los restantes elementos químicos? ¿Y las moléculas?
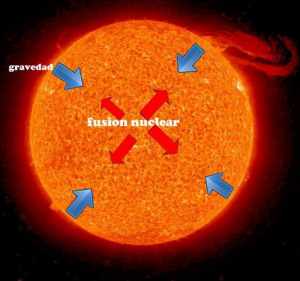
En el interior del Sol, al igual que en las restantes estrellas, se producen reacciones de fusión nuclear, en que los núcleos de hidrógeno (es decir, protones) se fusionan y dan núcleos de helio (constituidos por dos protones y dos neutrones), emitiéndose dos positrones, dos neutrinos y energía.
 Pero si la síntesis estelar hubiera culminado con la producción de helio (que también generó la gran explosión inicial), y éste hubiese permanecido confinado en el interior de las estrellas, no habría historia interesante que contar, ni nosotros estaríamos aquí.
Pero si la síntesis estelar hubiera culminado con la producción de helio (que también generó la gran explosión inicial), y éste hubiese permanecido confinado en el interior de las estrellas, no habría historia interesante que contar, ni nosotros estaríamos aquí.
Tras una etapa muy dilatada de fusión del hidrógeno, en la que el helio se va acumulando en la zona central, la estrella experimenta un cambio drástico.
La zona central de la estrella se contrae y se calienta, a medida que van encerrándose los nucleones (conjuntos de núcleos de helio) de cuatro en cuatro en los núcleos de helio sintetizados.
La temperatura y la densidad del núcleo aumentan para que se mantenga el equilibrio de presiones. Considerada globalmente, la estrella se hace menos homogénea.
Las reacciones nucleares hasta entonces imposibles se convierten en fuente principal de energía. Y la energía que producen las reacciones nucleares es enorme, del orden de un millón de veces la de una reacción química ordinaria.
Esto se refleja también en las unidades utilizadas: la unidad de energía nuclear es el megatón, que equivale a un millón de toneladas de explosivo químico.
Esta reserva de energía permite que la estrella mantenga su actividad durante unos 10.000 millones de años.
El Sol, por ejemplo, ya tiene cerca de 5.000 millones de años, es decir, ha recorrido menos de la mitad de su vida.
A medida que el gas se va acumulando para formar una estrella, lo primero en constituirse es un disco giratorio de gas y de polvo.
Mientras la estrella se condensa, e polvo se aglutina y crea planetas rocosos, como la Tierra El gas remanente se acumula y origina grandes planetas gaseosos como Júpiter.
Pero lo más interesante es que las cenizas de la combustión nuclear, más allá de la energía producida, no son otra cosa que los elementos de la tabla periódica, que son los materiales que constituyen a los seres vivos.
Con la contracción del núcleo estelar de una estrella producida a medida que ésta envejece (estrella gigante roja), el horno central gana en densidad y calor. Y este aumento de temperatura de la zona central hace que se produzcan fusiones con contactos breves entre núcleos de helio.
La colisión de dos núcleos de helio origina iniciamente una forma de berilio muy inestable, constituida por cuatro protones y cuatro neutrones.
Otro núcleo de helio choca con este blanco efímero y crea un átomo de carbono. La síntesis de carbono es el resultado de una delicada coincidencia entre las energías del helio, del berilio inestable y del carbono resultante. El oxígeno se origina, a su vez, por la fusión de carbono con un núcleo de helio.
En algunas estrellas gigantes rojas, la materia del núcleo, enriquecida con carbono, se desplaza convectivamente hacia las zonas exteriores, pudiendo escapar de la estrella para formar una especie de capullo de grafito.
El combustible acaba por agotarse el corazón o núcleo experimenta una suerte de congelación, convirtiéndose en una enana blanca. Y una enana blanca no cae en el colapso gravitatorio debido a la presión cinética de los gases (el oxígeno y el carbono se hallan en estado cristalino), sino que la presión gravitatoria se equilibra con la repulsión cuántica de sus electrones libres.
La elevada temperatura de la zona central de la enana blanca hace que ocurra una mayor diversidad de reacciones nucleares. La fusión del oxígeno origina azufre y silicio, y la del silicio fabrica hierro.
Una vez que la estrella que ha fabricado un núcleo central de hierro, no hay forma de generar energía mediante la fusión.
La estrella radiando energía a una velocidad asombrosa, se comporta como un adolescente con tarjeta de crédito, consume sus recursos a gran velocidad y se pone al borde del desastre. ¿Qué sucede entonces?
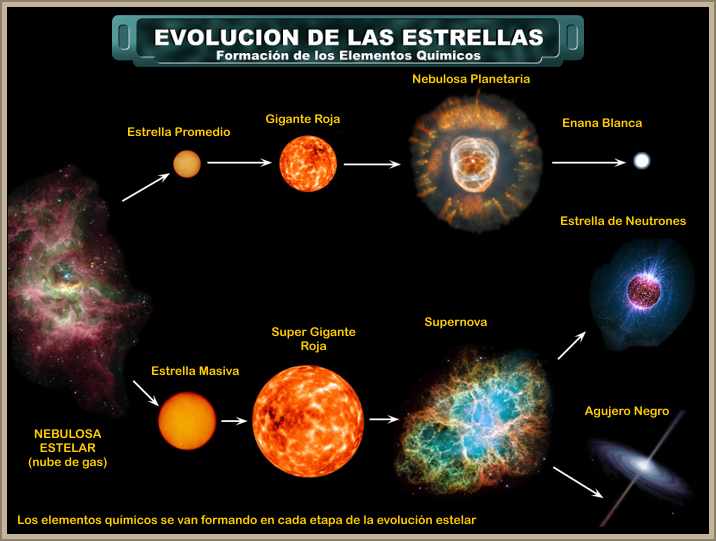
La explosión de una supernova: el núcleo estelar se colapsa en un segundo y se convierte en una estrella de neutrones o un agujero negro.
La materia de dicha zona central alcanza la densidad de los núcleos atómicos y no se puede comprimir más. Se produce una onda de choque que, al llegar a la superficie, produce la explosión de la estrella. La energía total desprendida viene a ser la que se podría emitir durante toda la vida del Sol.
Estas explosiones de supernovas desempeñan un papel especial en el enriquecimiento químico del Universo.

En su avance a través de las estrellas, la onda de choque de la supernova va provocando la síntesis de nuevos elementos.
Así van apareciendo todos los restantes, como el uranio, que son sintetizados gracias a estas ondas.
Violentas explosiones esparcen entonces los elementos, una vez formados, por el espacio interestelar. Y la atracción gravitatoria, por su parte, los moldea en nuevas estrellas y planetas, y el electromagnetismo construye con ellos las moléculas de la vida.
¿Cómo?. En una galaxia espiral, como la Vía Láctea, el gas interestelar se aloja preferentemente en los brazos. La presencia de polvo en el gas dificulta las observaciones ópticas, pues absorbe buena parte de la luz que atraviesa.
ero el polvo, al proteger de la luz ultravioleta los átomos de hidrógeno favorece su combinación en moléculas de hidrógeno, H2. En estos recóndictos remansos de las galaxias se acumulan también otras molécuas como el agua, el monóxido de carbono y el amoníaco. La variedad química de estas moléculas nos sorprendería.
Entonces, podemos afirmar que la composición química de la Tierra es un producto natural secundario de la generación de energía en las estrellas y de los sucesivos ciclos de nacimiento y muerte de estrellas en nuestra galaxia.
El estudio de los elementos químicos presentes en el Universo se realiza principalmente aplicando métodos a distancia". El análisis espectroscópico es uno de los más utilizados. Su origen se remonta a 1666 cuando Isaac Newton separó la luz blanca proveniente del Sol en los colores que la componen, haciéndola pasar a través de un prisma.
Esta dispersión de la luz blanca da origen al espectro visible, pequeña sección del espectro total de radiaciones electromagnéticas.
Hoy en día se utilizan aparatos más sofisticados, como los espectcrógrafos y espectrómetros, que son capaces de detectar tanto las radiaciones visibles como las de otras regiones del espectro electromagnético. Con la ayuda de estos instrumentos se están obteniendo datos interesantísimos acerca de la composición elemental del Sol, de los planetas solares y de estrellas muy lejanas a la Tierra.
![]()

HISTORIA DE LOS ELEMENTOS QUIMICOS: En la Edad Media, los alquimistas, antecesores de los químicos, tenían como meta fundamental modificar su ser interior para alcanzar un estado espiritual más elevado y pensaban que con la transmutación de los metales en oro podían lograrlo. Esta transmutación, conocida como la Gran Obra, debía realizarse en presencia de la piedra filosofal, cuya preparación fue la tarea que se impusieron los alquimistas.
En el siglo XIII, el objetivo de la alquimia incorporó la búsqueda del elixir de la larga vida, infusión de la piedra filosofal, que debía eliminar la enfermedad y prolongar la vida.
Durante el siglo XVII, a un alquimista alemán, Henning Brand , se le ocurrió la idea de que para encontrar la piedra filosofal debía fabricar oro a partir de la orina humana (¿quizá por el color?). Juntó durante varios días cinco litros de orina y la calentó hasta la ebullición luego de dejarla reposar durante dos semanas.
Al final, después de eliminar toda el agua, le quedó un residuo sólido. Brand mezcló este residuo con arena, lo calentó fuertemente y recogió los vapores que salían en un recipiente vacío.
Al enfriarse el vapor, sobre las paredes del recipiente se formó un sólido blanco: ¡cuál sería su asombro al ver que aquella sustancia brillaba en la oscuridad!
Brand había aislado el fósforo (del griego, "portador de luz"). El fósforo resplandece porque se combina lentamente con el oxígeno del aire, proceso durante el cual emite energía luminosa. Brand no conocía las propiedades del fósforo, pero aislar un elemento en 1669 resultó un descubrimiento espectacular.
En el siglo XVII el interés de los químicos se centraba en el descubrimiento de nuevos elementos gaseosos, y así fue como, entre 1766 y 1774, Henry Cavendish (1731-1810) identificó el hidrógeno, Daniel Rutherford (1749-1819), el nitrógeno y Cari Scheele (1742-1786), el cloro.
Además, al calentar mo-nóxido de mercurio, Joseph Priestley (1733-1804) obtuvo dos vapores: uno se condensó en gotitas, el mercurio, pero el otro, ¿qué era?. Priestley juntó ese gas en un recipiente e hizo algunos ensayos: si introducía una astilla de madera, ardía; si acercaba ratones vivos, éstos se volvían muy activos. En vista de lo cual, Priestley inhaló un poco de ese gas y notó que se sentía muy "ligero y cómodo".
A este gas lo llamó aire deflogistizado; hoy sabemos que era oxígeno.
Sin saberlo, Priestley fue la primera persona que usó la mascarilla de oxígeno.
¿Cuál es el resultado?

La lista de elementos aislados e identificados se amplió a través de los años y en el siglo XIX surgió la necesidad de ordenarlos. Estos y otros descubrimientos realizados por innumerables científicos, sumados a las nuevas tecnologías, hoy permiten afirmar que, de alguna manera, las metas de los alquimistas se han alcanzado. Los químicos son capaces de sintetizar sustancias que benefician a la humanidad de múltiples formas.
Por ejemplo, se han obtenido casi 1.500 isótopos radiactivos artificiales, que se usan en medicina y en la industria.
El elixir que cura todas las enfermedades no se ha obtenido, pero sí se han sintetizado decenas de miles de productos para combatir y prevenir enfermedades y que han aumentado la expectativa y la calidad de vida del hombre.
Fuente Consultada:
QUIMICA I - Sistemas Materiales - Estructura de la Materia - Mónica P. Alegría, Alejandro Bosack, Alejandra Dal Fávero y otros Editorial Santillana
¿Te apasiona la historia? No te pierdas esto:
⚓ Te puede interesar: Explorando otras ideas
¿A qué película pertenece esta imagen?






