Biografía de Pauli Wolfgang: El Principio de Exclusión
BIOGRAFÍA DE PAULI, WOLFGANG
Físico austríaco-estadounidense
Wolfgang Pauli (1900-1958), físico estadounidense de origen austríaco, premiado con el Nobel y conocido por su definición del principio de exclusión en mecánica cuántica.
Además su hipótesis, en 1931, de la existencia del neutrino, una partícula subátomica, constituyó una contribución fundamental al desarrollo de la teoría mesónica.

Pauli formuló el principio de exclusión, que establece que dos electrones no pueden ocupar el mismo estado energético de forma simultánea en un átomo. Por este descubrimiento recibió, en 1945, el Premio Nobel de Física.
Se doctoró en 1921 en la Universidad de Munich y fue asistente en la Universidad de Gotinga. Continuó su formación en Copenhague, bajo la tutela de Niels Bohr.
Trabajó inicialmente en la Universidad de Hamburgo y, luego, se mantuvo por espacio de veinticinco años como profesor de física teórica en la Escuela Politécnica Federal de Zurich.
Se le distingue como uno de los fundadores de la mecánica cuántica, junto con Heisenberg y Planck; adquirió gran prestigio por su principio de exclusión, enunciado en 1924, conocido también como principio de Pauli, según el cual dos partículas similares no pueden existir en el mismo estado, es decir, que ambas no pueden tener la misma posición y la misma velocidad, dentro de los límites fijados por el principio de incertidumbre de Heisenberg.
En otros términos, en un mismo átomo no pueden existir dos electrones con el mismo conjunto de números cuánticos -sabiendo que cada átomo queda descrito por completo una vez se han especificado sus cuatro números cuánticos- de donde resulta que al menos uno de ellos debe ser diferente.
Mediante el Principio de Pauli se logró interpretar las propiedades químicas de los elementos cuando se agrupan ordenadamente por su número atómico creciente.
Pauli recibió el premio Nobel de física a la edad de 45 años, en 1945, "por el descubrimiento del principio de exclusión". Al año siguiente, recibió la nacionalidad norteamericana y trabajó a partir de ese momento en el Instituto de Estudios Avanzados de Princeton, regresando posteriormente a Zurich.
DESCRIPCIÓN DE LA UBICACIÓN DE LOS LOS ELECTRONES EN UN ÁTOMO:
El núcleo y la disposición de los electrones a su alrededor, son los componentes cruciales que dictan la forma como se comporta un elemento.
Si pudiésemos tomar millones de fotografías de los electrones que orbitan alrededor del núcleo de un átomo, éstos aparecerían cada vez en una posición ligeramente diferente.
Las distintas posiciones forman series de hasta 7 anillos de nubes u "órbitas" alrededor del núcleo, donde las posibilidades de encontrar un electrón son altas.
En los átomos más pequeños, hidrógeno y helio, existe sólo una pequeña órbita cercana al núcleo.
Los átomos del helio tienen dos electrones y los del hidrógeno uno, por lo que la opción de hallar un electrón en un punto determinado de esta órbita es dos veces mayor en el átomo de helio que en el de hidrógeno.
Existe siempre un límite al número de electrones que cada órbita puede albergar.
En la órbita interior hay espacio sólo para dos, por lo cual, si un átomo tiene más electrones, éstos se desplazan a una segunda órbita, más retirada del núcleo. Esta segunda órbita puede albergar hasta 8 electrones.
La tercera también puede mantener 8 electrones, e incluso más -hasta 18-,si existe otra órbita. Sólo excepcionalmente la órbita externa presenta más de 8 electrones.
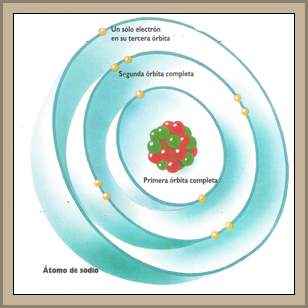
Los átomos con 8 electrones en su órbita externa son muy estables y lentos para reaccionar con otros elementos, debido a que se requiere mucha energía para adicionar un electrón o para desplazarlo.
Los átomos con un solo electrón en su órbita externa, como los del hidrógeno, sodio y potasio, son muy reactivos debido a que su electrón se remueve con facilidad.
de igual modo, los átomos a los que les falta uno de los 8 electrones son muy reactivos, pues aceptan con rapidez otro electrón en su órbita externa.
El fluoruro (un átomo de flúor con un electrón obtenido de otro átomo) que encontramos en la crema dental protege los dientes al eliminar y remplazar un componente del esmalte dental que es afectado por los ácidos en los alimentos.
Fuente Consultada:
Historia Universal de la Civilización Editorial Ramón Sopena Tomo II del Renacimiento a la Era Atómica
Temas Relacionados:
Leyes de la Teoría Atómica: Masa Atomica, Mol y Numero de Avogadro
La Vida Media de un Isotopo Quimico
La Maquina de Dios: Acelerador de Particulas
Teoría de Desintegración Nuclear del Átomo
El movimiento browniano estudiado por Albert Einstein
Cálculo del Radio de la Orbita en el Átomo de Hidrógeno
Nanociencia y Nanotecnologia:Que es la Nanociencia
Enlace Externo:• Wolfgang Pauli - Escuelapedia





