Historia de la Energia Nuclear:Resumen del Descubrimento
Historia de la Energía Nuclear
Descubrimiento Energía Atómica
Temas Tratados:
1-La Explotación Nuclear
2-Historia de la Energia Nuclear
3-Científicios Que Estudiaron El Atomo
4-Descripcion del Atomo Elemental
5-Accidentes Por La Manipulacion de Energia Nuclear
6-Enlaces a Temas Relacionados
7-Usos de la Energia Nuclear
La explotación de la energía nuclear fue la culminación de varios avances en el conocimiento del átomo.
Hay dos formas posibles de extraer energía de los núcleos atómicos: la fisión (división de núcleo) y la fusión (unión de núcleos atómicos).
Si se logra controlar, esta última ofrece la posibilidad de obtener energía limpia e ilimitada, pero hasta hoy sólo la fisión ha servido para producir energía.
Los principios de la fisión nuclear se estudiaron en la década de 1930 y se ensayaron durante la Segunda Guerra Mundial.
Las bombas de Hiroshima y Nagasaki dependían de una reacción en cadena de fisión incontrolada, fenómeno identificado por primera vez en 1933 por el húngaro Leo Szilard.
El principio era sencillo: en una muestra bastante densa de material (masa crítica), los neutrones de alta energía que escapan debido a una desintegración nuclear provocan otra, que libera nuevos neutrones de alta energía, y así sucesivamente, en una desintegración instantánea de todo el material que provoca una deflagración descomunal.
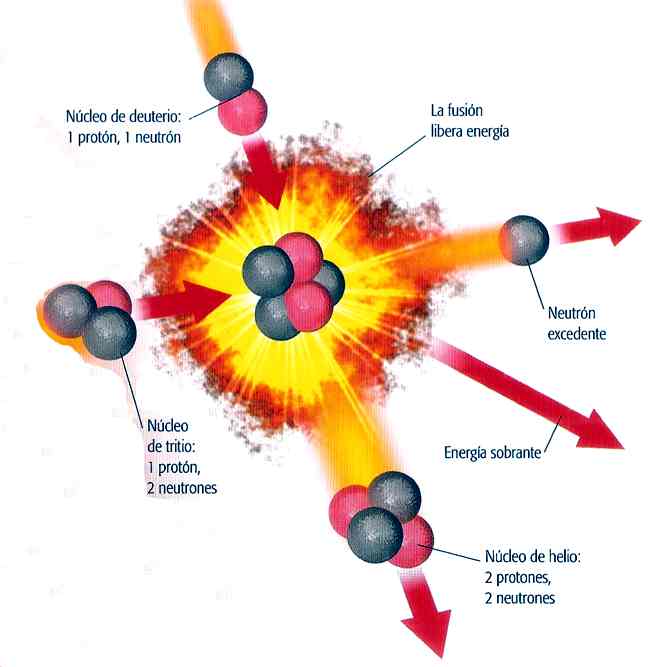
La fisión nuclear controlada requiere núcleos de combustible radiactivo enriquecido, moderados normalmente por otro material, como agua o grafito, que ralentiza el movimiento de los «neutrones rápidos» liberados y aumenta la probabilidad de que interactúen con otros átomos y sostengan la reacción en cadena.
Unas barras moderadoras de materiales que absorben neutrones se insertan o retiran para modificar el flujo de neutrones y la velocidad de la reacción.
Las centrales nucleares se diseñan de forma que la reacción se detenga automáticamente en caso de fallo catastrófico.
La energía se suele extraer permitiendo que la reacción caliente agua en la pila del reactor.

Historia de la Energía Nuclear
Cuando el hombre primitivo, frotando entre sí dos trozos de madera seca, obtuvo por primera vez pequeñas y amarillentas llamas, hizo el gran descubrimiento que habría de gravitar por los siglos de los siglos en la historia de la humanidad.
Instintivamente realizó la primera liberación de energía: la energía química acumulada por el Sol en forma de luz y calor, y echó las bases de la civilización.
Desde entonces, el progreso del hombre ha dependido de su habilidad para desentrañar y superar los secretos de la naturaleza.
Pero el hombre jamás se declara satisfecho de sus conquistas.
Lo desconocido constituye en todo momento para él un desafío permanente que le apasiona y estimula.
Una ambición suya hondamente sentida fue y sigue siendo descifrar la incógnita de lo misterioso.
Y nada más misterioso que la materia.
Los filósofos de la antigüedad forjaron sobre ésta definiciones diferentes.
Demócrito de Abdera (470-380 a. de J.C.) afirmó que se componía de "átomos", partículas diminutas, inalterables e indivisibles, y Dalton (1802), fundador de la teoría atómica, sostuvo muchos siglos después lo mismo.
A partir de entonces, el átomo se convirtió en la atracción de una legión de investigadores, pero fue Rutherford quien, en 1911, reveló su enigmática arquitectura.
La materia se compone de moléculas cuyo diámetro es de dos diezmillonésimas de milímetro, y átomos tan increíblemente pequeños que diez millones de ellos podrían colocarse en fila dentro del punto con que termina esta oración.
Durante muchos siglos se creyó que el átomo era el constituyente último e indivisible de la materia; mas ahora se sabe que semeja a un sistema solar ultraminúsculo y que se compone de un núcleo, correspondiente al Sol, y de electrones que giran alrededor del núcleo como planetas.
Este, que no es sólido o macizo ni uniforme, está formado por "protones", partículas cargadas de electricidad positiva; "electrones", partículas de electricidad negativa que giran como un torbellino en torno al protón, y "neutrones" que carecen de carga eléctrica.
Hay tantos átomos en una gota de agua que si todos los habitantes del mundo se pusieran a contarlos rápidamente y lo hicieran día y noche sin interrupción, necesitarían 10.000 años para terminar la cuenta.
Todos los átomos poseen una misma estructura general, misteriosamente conservada por ciertas fuerzas internas, pues los protones que están en el núcleo, cargados de electricidad positiva, deberían repelerse unos a otros violentamente, y no lo hacen.
Prueba de que existe alguna otra energía aún desconocida que los mantiene unidos, dando estabilidad al núcleo.
Los principios relacionados con la misma fueron intuidos por algunos estudiosos de la antigüedad, que contemplando ciertos fenómenos no supieron explicarlos de otra manera que por la acción de esas fuerzas misteriosas.
Se lanzaron algunos de ellos en su búsqueda pero, sin los elementos que la técnica incorporó siglos después a la acción de la ciencia, sólo lograron entrever lo que sería privilegio de los científicos modernos: El llegar a descubrir y luego darle aplicación.
CIENTIFICOS E INVESTIGADORES DE LA ENERGIA NUCLEAR: La historia de la energía nuclear consta de etapas, al frente de cada una de las cuales figuran, entre otros, estos nombres: Rutherford, los Curie, Becquerel, Soddy, Geiger, Moseley, Chadwick, Aston, Thomson, Bothe, Becker, Anderson, Blachett, Fermi, los Joliot-Curie, Urey, Murphy, Cockoroft, Walton, Lawrence, Kapitza, Otto Hahn, Lise Meitner, Frisen, Niels Bohr, Szilard, Tronstad, Wigner, Compton, Wheeler, Allison, Oppenheimer, Dunning, Smyth, Oliphant.

![]()
Y como denominador común de tanto esfuerzo, Einstein, científico genial y buen matemático, cuya ecuación "E = mc2", la más célebre ecuación científica (la energía es igual a la masa multiplicada por el cuadrado de la velocidad de la luz), revolucionó la concepción corriente sobre el universo y suministró algo más que la base teórica para la desintegración del átomo.
La nacionalidad de cada uno de esos hombres importa poco, pues la ciencia, para quien las fronteras no existen, es evolucionista y depende de la interasociación de las ideas.
La genealogía de los grandes descubrimientos científicos muestra que cada hombre de ciencia hereda un tanto de sus predecesores, al margen de la latitud geográfica en que naciera.
Fue a mediados del siglo XIII cuando aprendió el hombre a transformar la energía liberada de las reacciones químicas en energía mecánica de movimiento: inventó la pólvora.
Y resulta irónico que ello tuviera más bien propósitos destructivos que constructivos.
Hacia fines del siglo XVII descubrió la manera de aprovechar la energía de combustión para realizar trabajos mecánicos, transformando agua en vapor, y tuvieron que transcurrir otros des siglos antes de que supiera que la energía liberada de la combustión podía utilizarse directamente, sin los intermediarios de agua y vapor, encendiendo una mezcla de aire y combustible pulverizado, en los cilindres del motor conocido actualmente como de combustión interna.
Este último hallazgo trajo otros muchos tras de sí, el más importante de todos: la liberación de la energía nuclear energía casi inimaginable en la cual radica el secreto del calor solar. Lo indivisible fue dividido y lo imposible fue hecho realidad.
EL DESCUBRIMIENTO DE LA FISION NUCLEAR
1938:SE DESCUBRE LA FISIÓN NUCLEAR: A mediados de los anos treinta, físicos de Alemania, Francia e Italia competían por ser los primeros en conseguir romper un átomo.
El físico francés Frédéric Joliot-Curie había iniciado la carrera al declarar que «las reacciones nucleares en cadena» conducían a la «liberación de enormes cantidades de energía aprovechable».
En 1935 había sido galardonado con el Premio Nobel (junto con su mujer, Irene Joliot-Curie) por el descubrimiento de la radiactividad artificial.
En Berlín, un equipo de investigación compuesto por Otto Hahn, Fritz Strassmann y Lise Meitner empezó a bombardear átomos de uranio con neutrones. Los científicos esperaban que el proceso diera lugar a elementos radiactivos más pesados similares al uranio.
En vez de esto, a finales de 1938, Hahn y Strassmann (Meitner, judía austríaca, había huido a Suecia después de que Hitler invadiera Austria en marzo) se sorprendieron al descubrir que su bombardeo sobre el uranio había dado lugar a un elemento mucho más ligero que el uranio, llamado bario.
Hahn y Strassmann enviaron sus resultados a Meitner, a Estocolmo, donde ella y su sobrino, el físico Otto Frisen, investigaron el misterio.
Llegaron a la conclusión de que el núcleo del uranio, en vez de emitir una partícula o un pequeño grupo de partículas, como se suponía, desarrollaba una «cadena» y luego se rompía en dos fragmentos ligeros prácticamente iguales, cuyas masas, unidas, pesaban menos que el núcleo original del uranio. La diferencia de peso se convertía en energía.
Meitner dio el nombre de «fisión» al proceso. Joliot-Curie descubrió que la fisión del uranio producía la liberación de neutrones adicionales que, a su vez, podían ser utilizados para romper otros átomos de uranio.
Se habían establecido las condiciones para el tipo de reacción en cadena que daría lugar a la bomba atómica.
Durante la guerra, Hahn y Strassmann permanecieron en Alemania. Hahn fue capturado por los aliados en la primavera de 1945 y, mientras se hallaba detenido en Inglaterra, se enteró de que había ganado el Nobel de Química de 1944.
Cuando aceptó el premio, el sentimiento de que había realizado un gran descubrimiento científico estaba empañado a causa de que la fisión había hecho posible la destrucción de Hiroshima y Nagasaki.
Después de la guerra, Hahn defendió con gran pasión el control de las armas nucleares.
Es con la creación del mundo el acontecimierto más extraordinario, porque se descubrió la fórmula para perfeccionarlo o para destruirlo.
La liberación de la energía nuclear persigue cinco objetivos esenciales:
1) transmutar unos en otros casi todos los cuerpos simples, realizando así el sueño de los alquimistas medievales;
2) dar a la medicina nuevas y poderosas armas para combatir las enfermedades más rebeldes;
3) suministrar nueves procedimientos de investigación que han conducido a grandes progreses en la fisiología de las plantas y animales, incluso del hombre;
4) crear muchas substancias nuevas y producir artificialmente casi todas las materias que se encuentran en la naturaleza;
5) utilizar la energía almacenada en el átomo para usos prácticos de la especie humana.
------------- 00000 ------------
Consecuencias nefasta: Desde los descubrimientos de Madame Curie hasta Einstein, pasando por Rutheford, Chadwick y toda una generación de investigadores que pusieron su ciencia, sin saberlo, al servicio de las manos ambiciosas y criminales de los gobiernos, no transcurrieron más de unas decenas de años.
Poco tiempo después de la fabricación de la primera bomba atómica, los radionucleidos (nucleo inestable) se han esparcido por la Tierra de manera que buena parte de los organismos vivientes (entre los que nos encontramos los seres humanos) presentan en sus tejidos acumulaciones patológicas de sustancias radiactivas sin saberlo.
¿Cómo ha sido posible tal «hazaña»?, ¿es factible que en tan corto lapso de tiempo el hombre haya podido desperdigar por la faz de la tierra tanta radiactividad? Les conmino a que lean atentamente la siguiente crónica de una esperpéntica muerte anunciada.
------------- 00000 ------------
Descripción Física del Atomo: Los Cuatro Tipos de Fuerzas en la Naturaleza
Una de las fuerzas fundamentales del mundo natural es la fuerza gravitatoria. Es la fuerza de gran alcance que más importancia tiene en el campo del movimiento de los planetas y de los cuerpos celestes en general.
Cuando se investigan las partículas más pequeñas, adquieren importancia las otras fuerzas fundamentales: la fuerza electromagnética , la fuerza fuerte (que mantiene unido el núcleo atómico) y la fuerza débil (que tiene que ver con la desintegración nuclear).
La palabra átomo viene de la antigua palabra griega para definir una partícula de materia tan pequeña que ya no se puede dividir.
En su teoría atómica de 1803, el químico británico John Dalton (1766-1844) definió el átomo como la partícula más pequeña de un elemento que conserva sus propiedades químicas. Con esta hipótesis —que todavía es válida actualmente— se pudo explicar algunos fenómenos.
Sin embargo, hasta el descubrimiento del electrón en 1897, a manos del físico británico J.J. Thompson (1856-1940), no se disponía de una descripción física del átomo.
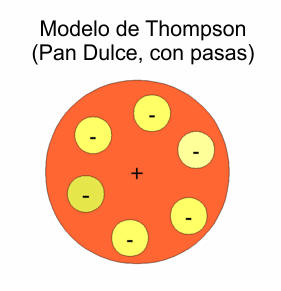
El físico inglés Ernest Rutherford (1871-1937) propuso un modelo atómico nuclear en 1911.
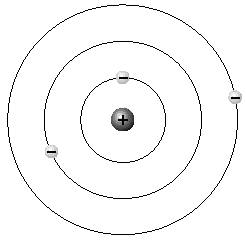
Se componía de un núcleo central denso y pequeño con carga positiva alrededor del cual orbitaban electrones cargados negativamente.
El núcleo contiene el 99,9 % de la masa atómica, aunque su diámetro es del orden de 10 elevado a -15 m., en relación al átomo, mucho más grande (aprox. 10 elevado -10 m).
El físico danés Nils Bohr (1885-1962) había sugerido que los electrones pueden moverse alrededor del núcleo en órbitas circulares o capas, pero que solamente eran posibles algunas órbitas.
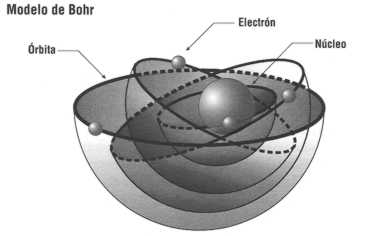
Esta teoría pudo explicar muchas características del espectro de la luz que emiten los átomos de hidrógeno excitados. Las longitudes de onda de las líneas espectrales guardan una relación con los niveles de energía de las órbitas posibles.
La teoría ondulatoria del electrón explicaría la razón de ser de los orbitales posibles, cuya circunferencia sería un múltiplo de la longitud de onda de los electrones.
Cuando Rutherford demostró experimentalmente que un átomo se ha de componer de un núcleo pequeño rodeado de electrones, surgió un problema fundamental.
Para no hundirse en el núcleo, los electrones tendrían que moverse en órbitas, como Bohr había propuesto,... asi empezó la maravillosa carerra científica por entender la estructura y funcionamiento del átomo.
------------- 00000 ------------
• ►PARA SABER MAS: LA ESTRUCTURA DEL ATOMO
Los primeros años del siglo XX presenciaron el nacimiento de la física nuclear, una nueva ciencia que tendría profundas consecuencias.
La estructura del átomo, con los electrones en torno a un diminuto núcleo central, quedó clara hacia 1911-1913, pero sólo gracias a la comprensión de la estructura del núcleo pudieron los científicos dominar la energía encerrada en el corazón del átomo.
El descubrimiento del núcleo reveló que la mayor parte de la masa del átomo y toda su carga positiva están concentradas en una pequeña región central.
En 1919, Ernest Rutherford había descubierto que los núcleos de varios elementos contenían partículas con carga positiva idénticas al núcleo de hidrógeno, el átomo más ligero.
Postuló entonces que estas partículas eran elementos constituyentes de todos los núcleos y les dio el nombre «protones».
Trece años más tarde, la imagen quedó completa cuando el físico británico James Chadwick descubrió el neutrón, una partícula eléctricamente neutra, apenas más pesada que el protón.
Juntos, los protones y los neutrones constituyen los núcleos atómicos de todos los elementos (excepto del hidrógeno, cuyo núcleo se compone solamente de un protón).
Los científicos saben actualmente que están ligados por la denominada fuerte fuerza nuclear.
En todos los átomos, el número de electrones (que determina las propiedades químicas del elemento) equilibra exactamente el número de protones del núcleo.
La función de los neutrones consiste en diluir la fuerza eléctrica repulsiva entre los protones, lo cual contribuye a la estabilidad del núcleo atómico.
En los núcleos más grandes, se requieren más neutrones para contrarrestar esta repulsión eléctrica; de esta forma, en los núcleos más pesados, el número de neutrones supera al de protones.
Sin embargo, sólo ciertas configuraciones de protones y neutrones resultan completamente estables.
Otras producen núcleos inestables o, en otras palabras, radiactivos.
Estos núcleos se transforman en estructuras más estables mediante la emisión espontánea de radiaciones: partículas alfa (núcleos de helio), partículas beta (electrones) y rayos gamma (fotones muy energéticos).
En determinadas circunstancias, un núcleo grande, como el de uranio, se puede dividir en dos fragmentos más o menos iguales y unos cuantos neutrones, en un proceso denominado fisión.
La energía liberada en el curso de estas transmutaciones es millones de veces mayor que la que interviene en las reacciones químicas, debido a la fuerza de las uniones nucleares.
A fines de los años 30, tras descubrir el fenómeno de fisión en el uranio bombardeado con neutrones, los físicos advirtieron que podían provocar una reacción en cadena, consiguiendo que los neutrones liberados en una fisión provocaran otras, y así sucesivamente.
Controlada, esta reacción en cadena constituye una fuente de energía útil; si se descontrola, determina una explosión devastadora.
Los físicos advirtieron muy pronto los potenciales usos y abusos de esta fuente de energía nuclear.
Sus sueños se han hecho realidad con la construcción de reactores que generan energía atómica para usos pacíficos; pero también se han hecho realidad sus más terribles pesadillas con la proliferación de armas atómicas.

Utilizando partículas alfa como «proyectiles», los físicos descubrieron que los núcleos contienen protones.
En la ilustración, varias partículas alfa dejan su rastro en un detector denominado cámara de nubes, según una fotografía de Patrick Blackett, tomada en Cambridge en 1925.
La partícula que está más a la derecha (compuesta por dos neutrones y dos protones) colisiona en el aire del detector con un núcleo de nitrógeno (siete neutrones y siete protones) y es capturada,
El núcleo absorbe los dos neutrones y uno de los protones, convirtiéndose así en un núcleo de oxígeno-1718 protones y nueve neutrones), pero rechaza el protón restante. Este sigue su trayectoria, describiendo la ramificación más tenue de la izquierda, mientras que el núcleo de oxígeno avanza muy poco más, dejando un trazo breve y grueso.

CRONOLOGÍA DE LOS ACCIDENTES POR MANIPULACIÓN Y EXPERIMENTOS
1897. Thomas Alva Edison trabaja en la investigación de los rayos X. Edison padece úlceras en ojos y piel.
1898. Los esposos Curie descubren el radio y el polonio.
1905. Los trabajadores que manipulan el radio presentan un nivel de espermatozoides inferior al normal.
1913. En Japón, el bar llamado «Marie Curie» invita a sus clientes a beber combinados de agua con radio.
1923. Tras avisar repetidamente del peligro de los rayos X, se hace pública la relación de un centenar de médicos y científicos que han muerto a causa de las radiaciones.
1934. Muere Madame Curie a causa de una leucemia.
1939. Tras las primeras escisiones del átomo del uranJo en el laboratorio, Albert Einstein envía una carta al presidente Roosvelt instándole en la necesidad de fabricar la bomba atómica.
1945. Estados Unidos lanza su primera bomba atómica con fines bélicos sobre Hiroshima.
1946. Estados Unidos lanza la segunda bomba atómica. Destino: Nagasaki.
1949. Estados Unidos (islas Marshall) y la Unión Soviética (Kazajstán) comienzan sus pruebas nucleares. Cerca de 8.000 curios de yodo 131 son vertidos a la atmósfera durante un experimento de fisión nuclear.
1950. Truman da la luz verde para la fabricación de la bomba H, a base de hidrógeno.
1954. Muere un miembro de la tripulación del barco de pesca japonés Dalgo Fukuryu Maru, expuesto a las radiaciones de la prueba de la bomba H en las islas Marshall.En el mes de marzo y en estas mismas islas, se produce la detonación de una bomba termonuclear de 15 megatones.
1957. A la vez que Gran Bretaña prueba su primera bomba H en la isla Christmas, un tanque de almacenamiento de residúos radiactivos explota en el centro de armas nucleares de los Urales (Unión Soviética). Once mil residentes son evacuados. El mismo año, un avión americano de transporte deja caer dos explosivos nucleares en el Atlántico que aún no han sido recuperados.
1958. Un bombardero B-47 sufre un accidente: la radiactividad se dispersa por la zona. Otro B-47 deja caer armas nucleares en Carolina del Sur: la población es controlada médicamente.Un reactor nuclear en Yugoslavia sufre un accidente: ocho empleados enferman. Cinco trabajadores mueren tras un fallo en el tratamiento de plutonio en el centro de investigación de Los Álamos.
1959. Un reactor atómico se pierde en medio del Atlántico. Años después se descubre que dicho reactor se deshizo en medio del océano.
1960. Francia comienza su carrera de pruebas atómicas con una explosión atmosférica en el Sahara.
1963. Un satélite de la Marina estadounidense sufre un accidente: el plutonio 90 penetra en la estratosfera y se disemina sobre doce países.
1964-1967. Más de diez accidentes nucleares en distintas partes del mundo siguen contaminando el aire y las aguas.
1969. Francia, que se había negado a firmar un tratado de interrupción de pruebas nucleares atmosféricas, lleva a cabo su primer experimento con bombas H en los atolones del Pacífico.Se produce un accidente en una fábrica de armas atómicas del norte de China y la radiactividad infesta la zona.
1970. En las cercanías del centro de pruebas atómicas de Nevada, aparecen enormes grietas en la tierra y un gran hongo nuclear se eleva alcanzando los 3 kilómetros de altura. Se evacúa urgentemente al personal, y 100 trabajadores sufren radiaciones.
1972. Un submarino nuclear soviético sufre una avería en su reactor al noroeste de Terranova. Se silencian las consecuencias.
1974. Se calcula en 1.600 millones de litros el material radiactivo vertido en el complejo nuclear de Hanford desde su apertura.En este año, la India lleva a cabo su primera prueba nuclear subterránea.
1975. Un oficial de la KGB revela que soldados soviéticos son obligados a introducirse en la zona altamente contaminada del lago Baikal. Tres cuartas partes de estos soldados murieron a causa de las enfermedades contraídas.
1977. Se detecta una alta proporción de casos de leucemia entre los 170.000 soldados que participaron en las pruebas nucleares de Nevada. El Gobierno propone indemnizaciones. Un camión derrama cerca de 20 toneladas de polvo de uranio en una autopista de Colorado.
1978. El satélite Cosmos 954, portador de un reactor nuclear, se estrella en un lago de Canadá.Se descubre que un equipo atómico emplazado por la CIA en el Himalaya produjo una fuerte contaminación en el río Ganges. Los habitantes de Utah exigen daños y perjuicios al Gobierno estadounidense por las lesiones ocasionadas por la lluvia radiactiva procedente de Nevada.
1979. Un portaaviones nuclear derrama 50 litros de agua altamente radiactiva en la bahía de San Diego.Francia prosigue sus pruebas atómicas en Mururoa, donde causa al menos dos muertos y varios heridos. En julio del mismo año, seis trabajadores franceses en el atolón resultaron heridos a consecuencia de una ola gigantesca provocada por una explosión atómica subterránea. En agosto se produjo un vertido de plutonio sobre el arrecife.
1981. La planta nuclear de Tsuruga, en Japón, vierte de manera descontrolada residuos directamente al mar.En el atolón de Mururoa un ciclón arrasó un depósito de residuos radiactivos: más de 20 kilos de plutonio cayeron al mar.
1983. Se hunde un submarino atómico soviético cerca de la península de Kamchatka.
1985. Se derrama la carga de uranio transportada por un camión en las cercanías de Dakota.El Rainbow Warrior, buque ecologista de Greenpeace, es hundido por una bomba colocada por el servicio secreto francés. Muere un tripulante.
1986. Estalla el reactor n.° 4 de la planta nuclear de Chernobyl. La contaminación se extiende por toda Europa. En Suecia, al otro lado del mar Báltico, la radiactividad destruyó una gran parte del habitat de los lapones y causó graves daños a la zona de granjas lácteas del centro del país.
1987. Se revela que entre 1945 y 1947 dieciocho personas fueron inyectadas con plutonio directamente en la sangre.Se produce un escape radiactivo en Darmstadt, Alemania Occidental.
1988. Escape radiactivo en un reactor japonés. Se hunde un barco que transportaba material radiactivo al norte de Gales.
1989. En Kíev, a 40 kilómetros de Chernobyl, la radiactividad dispara las agujas de los detectores. En dicha ciudad se controlan periódicamente a más de medio millón de ciudadanos, realizando tratamientos similares a los seguidos en Hiroshima y Nagasaki.Se detectan anormalidades cromosómicas entre los habitantes de Ucrania. Se informa de al menos 250 muertos entre los empleados de la central de Chernobyl. Se incendia la central nuclear española de Vandellós I. Las autoridades guardan un celoso silencio sobre las con secuencias del accidente. A la vez, organismos internacio nales califican el suceso como «el más grave después de Chernobyl».
1990. Se demuestra la relación entre exposición a la radiactividad de los padres y leucemia en su descendencia.Un diario austríaco informa de 6.000 muertes por can cer de tiroides tras la catástrofe de Chernobyl.El Soviet Supremo estudia un plan para evacuar 200.000 personas de las zonas circundantes a Chernobyl.Unas 125.000 personas pudieron ser contaminadas en la explosión de la central nuclear de Kazajstán.En una conferencia internacional en Polonia, científico soviéticos reconocen que en el futuro miles de personas fallecerán por los efectos de las radiaciones vertidas al exterior en el desastre de Chernobyl.
1991. Se producen tres accidentes nucleares en Japón: Fukulk, Onagwa y Kashiwazaki.Escape en un silo de armamento nuclear en Dakota del Norte.
Se detectan tres fugas radiactivas en la central nuclear de Kozloduj, en Bulgaria.Greenpeace denuncia la existencia de vertidos nucleares en el océano GlaciarÁrtico. Accidente en el acelerador nuclear del Hospital Clínico de Zaragoza. Dieciocho personas reciben radiaciones.
1992. La antigua Unión Soviética vierte residuos radiactivos en el mar de Kara. Accidente en la central nuclear de Sosnovi Bor, cerca de San Petersburgo. Suecia registra los efectos de la fuga radiactiva. Escapes nucleares en las centrales de Kozloduj (Bulgaria) e Ignalina (Lituania).Se encuentra polvo radiactivo procedente de Chernobyl en una perforación del casquete glaciar en Groenlandia.Los efectos mutagénicos del cataclismo de Chernobyl causan una intoxicación aguda a más de 1.000 personas en Rusia y Ucrania, tras ingerir unas plantas afectadas. 1993 en adelante. Francia continúa su campaña de pruebas nucleares en el atolón de Mururoa.
El comandante Cousteau y su tripulación fueron testigos de dichas pruebas nucleares, tras las que se sumergieron a una profundidad de 200 metros: el coral estaba agrietado y a través de estas fisuras se detectaron fugas radiactivas. Nadie osa permanecer dentro del agua más de cinco minutos en las playas de Mururoa si no quiere lucir unas erupciones rojas en la piel que permanecen durante días y causan unos grandes picores. Prosiguen los vertidos radiactivos. Los contenedores de material nuclear no parecen cumplir las condiciones mínimas de seguridad.
1997. Después de más de 200 pruebas atómicas, Francia expresa su intención de abandonar dichas prácticas.Se detecta aún un alto nivel de radiactividad en un amplio radio alrededor de la central nuclear de Chernobyl. El comandante Cousteau muere.
-------- 0000 --------
Temas Relacionados:
Rayos Catódicos
Einstein: E=mc²
Radioactividad I
Polonio y Radio
Radiactividad II
Fermi: Pila Atómica
Bomba Hiroshima
Mas Post Sobre Energias
Usos de la Energia Nuclear Aplicaciones y Beneficios
Nuevas Fuentes de Energia en el siglo XIX Petroleo y Electricidad
El Cuanto de Energia:Fisica Cuantica, La Constante de Planck
Fuentes de Energía No Renovables: Carbón y Petroleo-Reservas
Historia de la Energia Nuclear Resumen del Descubrimento
Concepto Físico de Energia: Tipos,Transformaciones y Ejemplos
Historia del Progreso Tecnológico En El Uso de la Energía
Ver Tambien: Composicion del Atomo, Electrones, Protones y Neutrones
Enlace Externo:• Historia de la energía nuclear






