El Tamaño del Universo:Medidas,Distancias y Escala Astronomica
El Tamaño del Universo:Medidas,Distancias y Escala Astronomica
Si se pudiera reducir el globo terráqueo al tamaño de una manzana, el hombre mediría en proporción una cienmilésima parte de milímetro.
Ante él cualquier ínfimo bacilo o bacteria alcanzaría dimensiones verdaderamente monstruosas.
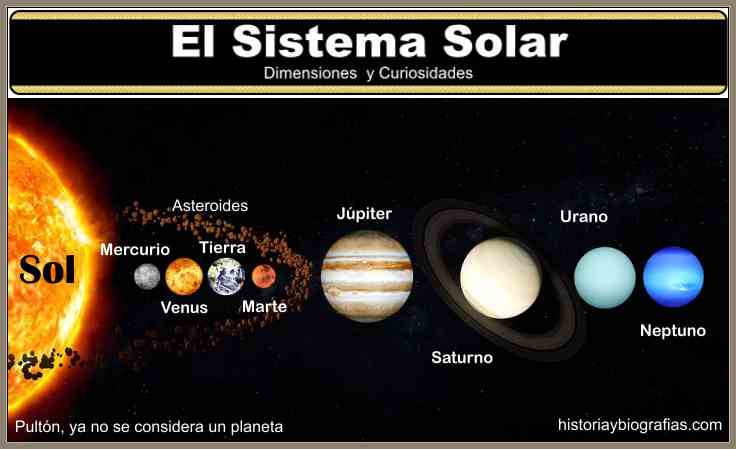
Por otra parte, como el Sol es una esfera de materia incandescente, que supera en ciento nueve veces el diámetro de la Tierra, si mantuviéramos las proporciones anteriores este Sol estaría representado por un globo de nueve metros de diámetro, situado a casi 1 Km. del planeta que, con el tamaño de una manzana, significaría la Tierra.
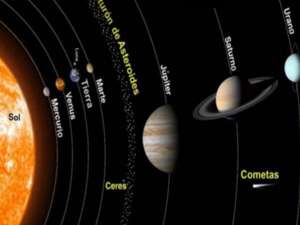
Pero en los límites de la familia solar, Plutón, el último y más distante de los planetas, figuraría como una bola de billar a 40 kilómetros del citado Sol del ejemplo.
Ahora bien; sobre la bóveda infinita del espacio brillan las estrellas, enormes masas globulares de gases ardientes.
La más próxima, denominada Alfa del Centauro, es otro sol similar al que nos ilumina, con casi su mismo peso y dimensiones.
Al igual que todas las estrellas. Alfa del Centauro no permanece inmóvil.
Surca el firmamento a una velocidad de 22 kilómetros por segundo, y debido a la enorme distancia que nos encontramos de ella, solamente a lo largo de siglos se apreciaría un movimiento casi imperceptible, puesto que dista de nosotros ¡42 billones de kilómetros!
Si se aplicara a esta distancia la misma proporcionalidad que se empleó al equiparar la Tierra con una manzana y se viera dónde habría que situar la estrella vecina, como se hizo con la distancia del Sol y Plutón, saltaría a la vista la imposibilidad de concretar el objetivo, ya que se necesitaría para esta escala un mapa de unos 260.000 kilómetros de amplitud, es decir, casi las dos terceras partes de nuestra distancia al satélite de la Tierra.
Se puede comprobar, de este modo, que la proporción entre la estatura de un ser humano y su distancia a la estrella más cercana es igual a la que existe entre un organismo ultramicroscópico y 260.000 kilómetros.
Un poco más distante, otra brillante estrella de azul tonalidad atrae nuestra atención.
Se trata de Sirio, notable por su magnitud en el espacio y por una estrellita que la acompaña y que constituyen con aquélla un sistema físico similar al que forman los planetas del sistema solar
El diámetro de Sirio es 1,8 veces el del astro mayor, lo que no significa mucho; sin embargo, situado en el lugar de éste proporcionaría 40 veces más luz y calor del que actualmente suministra.
• El Misterio Revelado
Con respecto a la diminuta estrella que gira en torno de Sirio corresponde aclarar someramente su singular historia.
Poco luminosa y lejana, fue ignorada durante siglos por los estudiosos, quienes por razones de tipo especulativo intuían su existencia.
Intentaremos explicarlo: la altura del Sol sobre el horizonte varía con la hora del día; del mismo modo, respecto del movimiento de las estrellas se puede establecer exactamente la hora correspondiente a un momento determinado.
Debido a su gran luminosidad Sirio era utilizada por los astrónomos como estrella horaria.
Pero en el firmamento ésta resultaba un astro poco puntual, que se retrasaba o adelantaba temporalmente.
Observaciones posteriores permitieron constatar que la estrella describía en el firmamento una levísima órbita elíptica.
Sin duda alguna, un astro perturbador, aún invisible, era el causante, con la atracción de su masa, del titubeante comportamiento de Sirio.
Apelando a la ley de la gravitación universal se admitió la existencia de un nuevo astro, cuya órbita y posición fueron determinadas en 1850 por el astrónomo alemán Frederick Peters.
En 1862, mediante el uso de un anteojo, a la sazón recién fabricado, se lo descubrió inesperadamente y comenzó a plantearse un nuevo interrogante referido a la especial naturaleza de la materia que lo compone.
La incógnita fue revelada en 1924, cuando el astrónomo estadounidense Walter Adams, empleando el interferómetro de Michelson, logró la doble comprobación del efecto Einstein, y la confirmación de la extraordinaria densidad (23.000 veces más que la del platino) de la diminuta estrella.
El "misterio" de la substancia radicaba en lo siguiente: en tamaño, el satélite de Sirio es sólo tres veces más grande que la Tierra, pero su masa es casi igual a la del Sol.
A fin de que toda esta materia pueda caber en tan escaso volumen hay que someterla a una intensa presión, comprimirla enormemente.
Los átomos, elementos que componen toda materia, tienen un límite de resistencia mecánica, tras lo cual son deshechos en un confuso montón de núcleos y electrones que invaden y desbordan los espacios interatómicos.
Roto el equilibrio interno del átomo, los espacios vacíos son cubiertos por los componentes de otros átomos triturados.
Así, el espacio ocupado disminuye y por lo tanto la densidad media (relación entre volumen y masa) se acrecienta.
Era éste, pues, el íntimo secreto que guardaba en su seno la estrella más brillante del cielo.
La "fuga" del universo
Se se miden las velocidades de esos universos-islas se llega a la conclusión de que parecen alejarse entre sí, acrecentando su velocidad a medida que se van distanciando.
Esta fuga desordenada no afecta las dimensiones propias de las galaxias, que, alejándose, siguen conservando su tamaño.
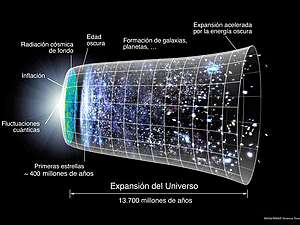
Habida cuenta de esto, y calculando el tiempo necesario para que todas esas islas estelares volvieran a juntarse marchando a idéntica velocidad, pero inversamente, se necesitarían unos 13.000 millones de años para volver a reunirse en un conjunto de estrellas distribuidas en un solo universo de manera uniforme.
Si a partir de este conjunto único de densidad estelar se han condensado en grupos de estrellas de modo similar a como suponemos que el gas primitivo se fue condensando en estrellas, sigue aún en pie uno de los tantos interrogantes que se plantea la astronomía, para cuya respuesta el hombre acude con su ciencia al más allá.
Con el misterio de la creación ha quedado atrás en el tiempo y sumida en las sombras del espacio, a 1.500 millones de años de luz, una imperceptible manchita nebulosa: es nuestro universo.
Confundido entre corpúsculos titilantes hay un sol que nos es familiar, y como un punto minúsculo, donde el hombre lucha por penetrar en el misterio de lo infinito, está la Tierra, nuestro planeta.


El Big Bang hace 15.000 millones de años
| MEDIDAS Y DISTANCIAS DEL UNIVERSO | |
| De la Tierra al Sol | 148,8 millones de Km. |
| Del Sol a la estrella más próxima, la Alfa Centauri | 4,2 años luz |
| Del Sol al centro de la Galaxia Vía Láctea | 25.000-30.000 años luz |
| Diámetro de la Galaxia Vía Láctea | 100.000 años luz |
| De la Galaxia Vía Láctea a Maffei I (la galaxia más lejana del Grupo Local) | 3,3 millones de años luz |
| Diámetro de Maffei | 100.000 años luz |
| De las galaxias más cercanas a la Galaxia Vía Láctea: | |
| Pequeña Nube de Magallanes | 196.000 años luz |
| Gran Nube de Magallanes | 210.000 años luz |
| Galaxias exteriores: | |
| Galaxia Andrómeda | 2,2 millones de años luz |
| Galaxia Vórtice | 37 millones de años luz |
| Galaxia Carretel | 500 millones de años luz |
| Galaxias más lejanas identificadas | >10.000 millones de años luz |
| Objetos más lejanos visibles (galaxias, quásares) | 15.000 millones a 20.000 millones de años luz |
| Diámetro estimado del universo | 1,5 millardos de años luz |
La mediciones indicadas mas abajo van variando según se logran técnicas
e instrumentos mas precisos para su medición
| Magnitud Visual | Distancia Años-Luz | Diámetro Años-Luz | |
| Vía Láctea | - | 97.800 | |
| Nube de Magallanes (mayor) | 0,9 | 156.480 | 32.600 |
| Nube de Magallanes (menor) | 2,5 | 182.560 | 26.080 |
| Sistema de la Osa Menor | - | 228.200 | 3.260 |
| Sistema del Escultor | 8,0 | 270.580 | 7.170 |
| Sistema del Dragón | - | 326.000 | 4.560 |
| Fornax | 8,3 | 619.400 | 21.520 |
| Sistema del León II | 12,04 | 749.800 | 5.220 |
| Sistema del León I | 12,0 | 912.800 | 4.890 |
| NGC 6822 | 8,9 | 1.500.000 | 8.800 |
| NGC 147 | 9,73 | 1.858.000 | 8.780 |
| NGC 185 | 9,43 | 1.858.000 | 7.500 |
| NGC 205 | 8,17 | 2.217.000 | 16.300 |
| NGC 221 (M 32) | 8,16 | 2.217.000 | 7.820 |
| IC 1613 | 9,61 | 2.217.000 | 15.300 |
| Andrómeda (M 31) | 3,47 | 2.217.000 | 130.400 |
| NGC 538 (M 33) | 5,79 | 2.347.200 | 55.420 |
| Maffei I | 11,0 | 3.260.000 | - |
| Estrella | Constelaciones | Magnitud Aparente | Distancia Año-Luz |
| Sirio + Canope + Rigil Kent Arturo Vega Rigel + La Cabra + Proción Achernar Hadar + Altair. Aldebarán + Acrux + Betelgeuse + + + Antares + La Espiga + Pólux Fomalhaut Deneb Mimosa Régulo + Adhara + Bellátrix Shaula Alnath | Alfa del Can Mayor Alfa de Argos (Carina) . Alfa del Centauro Alfa del Boyero Alfa de la Lira Beta de Orión Alfa del Cochero (Auriga) Alfa del Can Menor Alfa de Erídano Beta del Centauro Alfa del Águila Alfa del Toro Alfa de la Cruz del Sur Alfa de Orión Alfa del Escorpión Alfa de la Virgen Beta de los Gemelos Alfa del Pez Austral Alfa del Cisne Beta de la Cruz del Sur Alfa del León Epsilón del Can Mayor Gamma de Orion Lamda del Escorpión Beta del Toro | -1,47 -0,71 -0,27 -0,06 0,03 0,08 0,09 0,34 0,49 0,61 0,75 0,78 0,80 0,85 0,92 0,98 1.15 1.16 1,26 1,28 1,33 1,42 1,61 1,61 1,64 | 8.7 300 4 36 26 850 45 11 75 300 16 65 270 650 400 220 35 23 .500 370 85 620 450 300 270 |
| (+):Estrella Doble (+++): Estrella Variable | |||
------------ 0000 ------------
LAS DISTANCIAS EN EL UNIVERSO
A medida que la Tierra gira sobre su eje, un punto sobre el ecuador se mueve a unos 1.600 Km. por hora.
En su giro alrededor del Sol, la Tierra recorre unos 30 Km. por segundo. En un día recorre más de 2. 500.000 Km.
Es bastante curioso comprobar que el diámetro de la órbita terrestre es casi exactamente mil veces mayor que la distancia recorrida por la luz en un segundo.
El recorrido anual de la Tierra alrededor del Sol es de casi mil millones de Km. Un niño de diez años de edad ha viajado casi diez mil millones de Km. aun cuando nunca haya salido de la localidad en que vive.
Al girar la Vía Láctea sobre sí misma, el Sol y sus planetas se mueven a unos 250 Km. por segundo. Aun así, el Sol necesita unos 200 millones de años para realizar un giro completo alrededor del centro de la galaxia.
Las galaxias se alejan velozmente unas de otras en el universo. Algunas de ellas recorren más de 100 000 Km. por segundo.
Se necesitaría más de un millón de esferas iguales a la Tierra para hacer una esfera igual a la del Sol.
Algunas de las grandes “llamaradas” que brotan del Sol (protuberancias solares) alcanzan una altura de varios cientos de miles de kilómetros. La más alta que se haya registrado tenía 1 600 000 kilómetros:
Se necesitarían 27 000 millones de soles para hacer una esfera tan grande como la estrella roja gigante llamada Epsilon de Auriga.
Cada hora, alrededor de un millón de meteoritos llega a nuestra atmósfera. Casi todos, salvo muy raras excepciones, se desintegran antes de llegar a la superficie de la Tierra. No obstante, los meteoritos pueden representar un verdadero peligro para los viajes espaciales.
En nuestra galaxia de la Vía Láctea existen por lo menos 200.000 millones de estrellas.
Se sabe que en el universo existen más de cien mil millones de galaxias.
Si todas las estrellas de la Vía Láctea tuvieran nombre, se necesitarían 4.000 años para decirlos todos, suponiendo que se pronunciara uno por segundo sin detenerse.
En todas las galaxias juntas debe haber, probablemente, tantas estrellas como granos de arena existen en todas las playas del globo terrestre.
La estrella más cercana a nuestro Sol está a 40 billones de Km. de éste.
Pese a los millones de estrellas existentes, el espacio no está ocupado en exceso. Se halla tan cubierto de estrellas como lo estaría América del Sur de ardillas si hubiera solamente tres de ellas corriendo por todo el continente.
La longitud de nuestra galaxia es de alrededor de 100 000 años luz (100 000 veces 10 billones de Km.).
Nuestro Sol está a unos 30.000 años luz (30 000 veces 10 billones de Km.) del centro de la Vía Láctea.
La Gran Espiral de Andrómeda es la galaxia más cercana a nuestra Vía Láctea. Está a una distancia de más de 2 millones de años luz (20 trillones de km).
Las galaxias más lejanas que pueden ser observadas con nuestros telescopios están a una distancia de unos 2 000 millones de años luz, aproximada mente.
La temperatura en la superficie del Sol es de 6 000 °C. En su interior alcanza a 14 millones de grados.
En un año, el Sol utiliza 22 trillones de toneladas de su hidrógeno para producir la energía que irradia. Pero, a pesar de esto, sus reservas de hidrógeno le permitirán existir todavía durante miles de millones de años.
La Nebulosa del Cangrejo es una inmensa nube de gas que se extiende a lo largo de 25 000 billones de Km. Desde hace 5 000 años, esta nebulosa crece a razón de 1.000 Km. por segundo.
Una cucharada de la materia que forma ciertas estrellas (las estrellas enanas) pesaría en la Tierra más de una tonelada.
La atracción de la gravedad en la superficie de la estrella enana que acompaña a Sirio (Sirio B) es 250.000 veces mayor que en la superficie de la Tierra.
Fuente Consultada: Mundorama Geografía General Tomo I
Temas Relacionados:
Big Bang
Origen de la Vida
Origen del Hombre
Teoría de la Evolución
Muerte de una Estrella
Los Pulsares Enana Blanca
Peso de Una Estrella de Neutrones
La Vida del Sol Tiempo de Vida Hidrogeno del Sol
La Luna Muestra Siempre la Misma Cara
Origen del aire que respiramos El Oxigeno
Enlace Externo: Descubre El Tamaño del Universo
¿Te apasiona la historia? No te pierdas esto: